기사본문
바이엘-록소 TRK 저해제..'환자 반응률 93%' 결과발표
입력 2017-12-05 15:14 수정 2018-11-22 13:51
바이오스펙테이터 김성민 기자
지난달 바이엘이 록소온콜로지가 가진 항암제에 대한 공동개발 협약을 체결한지 한달 만에, 그 성과가 부각되고 있다. 바이오마커를 기반으로 한 새로운 패러다임의 약물로 TRK(Tropomyosin receptor kinase) 억제제인 '라로트렉티닙(larotrectinib, LOXO-101)'과 'LOXO-195'의 개발 및 상업화를 위한 제휴계약 체결로 최대 15억 달러 규모에 달하는 딜이었다.
록소는 지난 4일 아틀란타에서 개최된 AACR(American Association for Cancer Research) 특별 컨퍼런스에서 소아환자를 대상으로 한 SCOUT 임상1상 결과를 발표했다(NCT02637687). 불응성(refractory) 고형암 혹은 CNS 종양, 영아 섬유육종(IFS)을 가진 1달~21살의 환자를 대상으로 했다.
놀랍게도 이들 환자에서 객관적반응률(Objective response rate)은 93%에 달했다. 구체적으로 부분반응(Partial response)은 67%, 완전관해(Complete response)는 27%다. 주요 부작용은 간수치(ALT) 상승, 백혈구감소증(leukopenia), 빈혈(anemia) 등으로 대부분 1~2등급에 그쳤으며, 4등급 이상의 부작용은 나타나지 않았다.
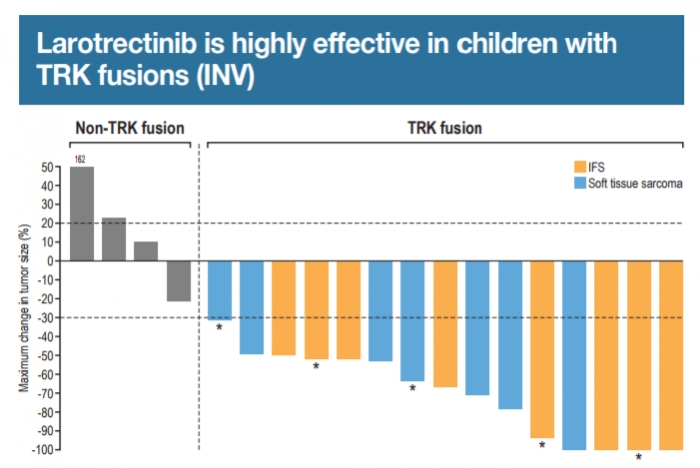
한가지 흥미로운 점은 TRK 융합형을 가진 환자에서 종양감소효과가 월등했다는 점이다. 바이오마커를 기반으로 한 항암제 연구개발이 중요하다는 것을 보여주는 임상결과다. 임상을 진행한 총 24명의 환자 중 17명은 TRK 융합형 환자(그래프 오른쪽), 7명은 TRK 융합형을 가지지 않은 환자(왼쪽)로 몇명의 환자는 아직 평가중에 있다.
TRK 융합형은 다양한 암종에 매우 드물게 발현하는 타입으로, TRK 시그널링이 망가질 경우 무분별하게 종양이 성장한다. 정상조직에는 거의 발현하지 않는다고 알려져 있다. 라로트렉티닙은 TRK 변이형인 TRKA, TRKB, TRKC를 억제하는 pan-TRK 억제제로 각 단백질에 대한 약물의 억제효율을 나타내는 IC50 값은 5~11nM다.
바이엘-록소는 글로벌 임상2상의 환자등록을 진행하고 있는 상태로, 적응증 타입은 임상1상과 동일하다.
록소가 지난 '미국임상종양학회(ASCO) 2017'에서 발표한 결과에 따르면 라로트렉티닙은 TRK 중합형변이를 가진 50명의 성인, 어린이 환자군을 대상으로 한 임상에서 약물반응률이 76%에 이르렀다. 당시 높은 반응률로 업계의 주목을 끌었고, 이번 임상에서도 동일선상의 결과를 확인한 것.
라로트렉티닙은 올해 미국식품의약국(FDA), 유럽의약품청(EMA)에 TRK 중합형변이를 가진 환자를 대상으로 신약승인신청서를 제출한 상태로 내년 중순에 신약승인을 받을 것으로 기대된다. 라로트렉티닙은 몇년 내 10억 달러의 매출을 올리는 블록버스터 약물이 될 것으로 전문가들은 예상하고 있다.
한편, 록소는 LOXO-101은 라로트렉티닙을 포함한 1세대 TRK 저해제 투여에 따른 내성환자를 대상으로 한 차세대 약물(LOXO-195)로 상1/2상을 진행하고 있다.







