기사본문
연대 연구팀, 악성 'EMT 위암' 타깃 표적항암제 물질 발굴
입력 2018-05-23 13:33 수정 2018-05-23 13:52
바이오스펙테이터 장종원 기자

▲연세대 김현석 교수(왼쪽), 정재호 교수(오른쪽).
국내 연구진이 난치성 위암을 타깃으로 하는 새로운 항암신약 후보물질을 발굴했다.
연세의대 김현석 교수 연구팀과 정재호 교수 연구팀은 23일 표적항암제와 면역치료제에 저항성을 가진 상피중간엽전이(epithelial-mesenchymal transition, EMT) 분자아형 위암에서 표적 항암물질 후보와 동반진단법을 발견했다고 밝혔다.
위암 치료 실패의 주요 원인 중 하나는 EMT 현상이다. EMT는 상피세포성 암이 중간엽세포 특성을 지닌 종양세포로 변형되는 것으로 치료제 내성이나 암세포의 전이를 유도하는 것으로 보고되고 있다.
아시아 암 연구그룹(Asian Cancer Research Group)에 따르면 모든 위암의 코호트 데이터에서 재발, 전이와 강한 상관관계를 보이는 EMT 분자아형에 속하는 환자들은 전체 위암 환자의 15%~43%에 이르고 이들의 5년 생존률은 30% 미만으로 가장 예후가 나쁜 환자군에 속했다.
현재 EMT 신호전달을 직접적으로 매개하는 여러 표적을 대상으로 표적의 기능을 떨어뜨리는 물질들에 대한 임상연구가 진행 중이다. 하지만 직접적으로 암 사멸 효과가 미미하거나 정상세포에 대한 부작용으로 임상에 적용하지 못하고 있다.
김현석 교수 연구팀은 자체 구축한 바이오마커-항암제 동시 개발 플랫폼을 이용해 1500여개의 임상약물 및 항암약물 스크리닝을 진행 EMT 분자아형 위암에 선택적 치료효과를 갖는 물질을 탐색했다. 탐색결과 효소 NamPT 기능을 억제하는 FK866이 합성치사(Synthetic lethality) 기전을 통해 NAPRT 효소의 발현이 억제된 EMT 분자아형 위암에서 선택적으로 항암효과를 가진다는 것을 발견했다.
NamPT와 NAPRT는 세포 생존에 필요한 에너지를 만드는데 필수적인 NAD(Nicotinamide adenine dinucleotide)의 생합성에 상호 보완적으로 관여하는 효소다. EMT 분자아형 위암의 경우 NAPRT 효소가 억제돼 있어 NamPT 효소를 통해 NAD를 합성하고 성장과 줄기세포를 유도한다. 따라서, NamPT 생성을 약물로 억제할 경우 에너지를 생성을 하지 못해 EMT 분자아형 암세포만 굶어죽게 된다.
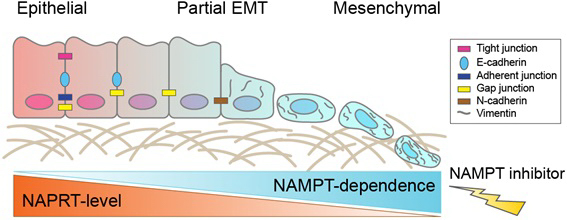
▲NamPT 저해제의 중간엽전이 (EMT) 분자아형 암세포에 대한 작용 기전
연구팀은 정재호 교수 연구팀이 자체적으로 확보한 환자유래 위암 이식 동물모델(PDX)을 활용해 생체내에서 FK866가 EMT 분자아형 위암의 종양 성장을 억제한다는 것을 검증했다. 또한, 세브란스병원 위암 환자 942명의 종양을 대상으로 면역화학염색분석을 통해 EMT 현상에서 암 전이를 억제하는 E-cadherin 단백질의 소실이 NAPRT 단백질 결핍과 매우 높은 상관관계를 가진다는 것을 확인했다.
추가적으로 연구팀은 암 빅데이터 분석을 통해 NAPRT의 발현억제가 위암뿐만 아니라 대장암, 췌장암의 EMT 분자아형에서도 광범위하게 나타나는 것을 밝혀 이번 연구를 통해 발굴한 NamPT 저해제를 여러 난치성 암종에 확대 적용할 수 있을 것으로 예상하고 있다.
김현석 교수는 “이번 연구는 표적 치료제, 면역치료제에도 저항성을 갖는 EMT 분자아형의 위암뿐만 아니라 같은 아형의 대장암, 췌장암이 갖는 아킬레스건을 최초로 발견한 것”이라며 “이들 암에 적용 가능한 치료 표적과 동반진단법을 동시에 제시한 것이 가장 큰 성과”라고 설명했다. 김 교수는 “이번 연구에서 발견한 FK866의 항암 효과를 극대화하고 부작용을 최소화 할 수 있는 신약 후보물질을 개발하는 후속연구를 진행 중”이라고 밝혔다.
한편 이번 연구는 국제학술지 가스트로엔터롤로지(Gastroenterology, IF 18.392) 온라인판에 게재됐다.







