기사본문
셀트리온 '램시마IV vs 램시마SC' 비교 3상 결과는?
입력 2019-06-17 10:25 수정 2019-06-18 08:12
바이오스펙테이터 조정민 기자
셀트리온이 환자의 투약편의성을 높이기 위해 피하주사형 제제로 개발된 램시마SC의 유효성과 안전성을 입증한 임상 3상 Part1, 2 결과를 최초로 공개했다. 셀트리온은 하반기 유럽 허가를 시작으로 램시마IV와 램시마SC를 활용한 투트랙 치료옵션(Dual formulation) 전략을 본격화할 계획이다.
셀트리온그룹은 지난 12일부터 15일까지 스페인 마드리드에서 열린 '2019 유럽 류마티스 학회(The European League Against Rheumatism; EULAR)'에서 램시마SC와 관련한 2종의 포스터를 발표했다. 특히 류마티스관절염 환자 362명을 대상으로 램시마SC 유효성의 비열등성을 확인한 임상3상 결과도 처음으로 공개했다. 바이오스펙테이터는 2종의 포스터를 통해 핵심 내용을 살펴봤다.
◇램시마IV vs 램시마SC 치료 효과 비교.."30주까지 동등한 치료효과, 비열등성 확인"
셀트리온은 램시마 정맥주사(IV)제형과 램시마 피하주사(SC)제형의 안전성과 유효성의 비열등성을 확인하기 위해 진행한 임상3상 결과를 발표했다. 이들은 총 362명의 류마티스관절염 환자를 대상으로 임상을 진행했다.
모집된 환자들은 0주와 2주째 3mg/kg 농도의 램시마IV를 적용받고, 6주 시점에 2주마다 램시마SC 120mg을 적용하는 군과 8주마다 램시마IV 3mg/kg를 적용하는 군으로 1:1 무작위로 배정됐다. 임상 시작 후 30주부터 54주까지는 모든 환자들에게 2주마다 SC제형 120mg을 적용했다. 연구진은 비열성 마진(Non inferior margin; NI margin)을 임의로(-0.6) 설정하고 특정 시점에서의 램시마SC와 램시마IV의 치료 효과를 평가, 분석했다. 일차 평가기준은 22주째 C반응성 단백질을 기준으로 하는 DAS28의 변화치였으며 ANCOVA 분석도구를 통해 분석을 진행했다.

▲램시마SC 120mg과 램시마IV 3mg/kg 간의 효능 을 비교한 결과 (셀트리온 2019 EULAR 포스터 발표자료)
치료 22주 시점에서 치료평가 및 관해(remission)를 판단하기 위한 질병 활성도 평가지표 DAS-28(Disease activity score 28)을 비교한 결과, SC제형은 2.22, IV제형은 1.95의 수치 변화가 확인됐다.
증상이 경감된 정도를 의미하는 지표인 ACR(Amerincan college of rheumatology)도 관찰했다. 20% 이상의 증상 완화를 나타내는 ‘ACR20’의 경우 SC제형이 2주와 6주, 22주의 관찰시점에서 IV제형과 유사했으나 30주에서는 더 높은 반응률을 보였다. ACR50과 ACR70 역시 비슷한 양상이 관찰됐다.
치료 시작 2주, 6주, 14주, 22주, 30주 시점에서 EULAR-CRP 반응률을 관찰한 결과에서도 질병의 개선정도를 평가했을 때, SC제형이 더 높은 수치를 보였다. 30주에 높은 치료반응(good response)을 보인 환자 비율을 살펴보면 SC제형은 51.5%, IV제형은 36%로 나타났다.
같은 약물이어도 제형이 변하면 약동학(PK)이 변하기 때문에 이를 확인하는 절차가 필수적으로 진행된다. 셀트리온은 SC제형의 PK 모델링 결과도 발표했다. 0~6주까지 SC제형과 IV의 혈중농도값은 비슷하게 유지됐는데 이는 0주와 2주에 IV제형 투약의 결과로 파악된다. 6주에서 14주동안 SC제형의 혈중농도는 약간 증가한 반면, IV제형은 점차 낮아졌다. 14주부터 30주까지 SC제형은 일정한 농도를 계속 유지하는 모습을 보였다. 회사 측은 SC제형의 경우 타겟하는 역치 농도인 1μg/ml에 비해 더 높은 수준의 농도를 30주까지 유지했다고 설명했다.
안전성 프로파일은 SC제형, IV제형 두 그룹이 유사한 것으로 나타났다. 약물과 관련된 이상반응이 나타난 비율은 SC제형이 25.3%(43명), IV제형이 21.3%(38명)이었다. 그 중 3등급(grade 3) 이상의 중증 이상반응이 나타난 것은 SC제형 0.6%(1명), IV제형 2.2%(4명)으로 SC제형이 더 우수한 안전성을 가진 것으로 관찰됐다. SC제형은 그 형태와 적용경로의 특성상 주입 관련 반응(infusion related reaction; IRR) 또는 전신적 주사 반응(systemic injection reaction; SIR) 등이 관찰되지 않았으며 부분적인 주사부 반응(localized injection site reaction) 역시 Grade 1~2의 경미한 반응이었다. 이러한 결과들은 램시마SC제형이 IV제형보다 환자들에게 투약편의성과 안전성을 제공한다는 것을 의미한다.
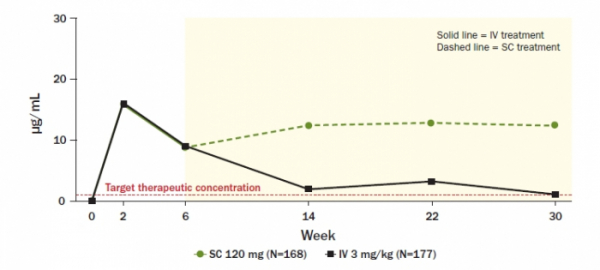
▲램시마SC와 램시마IV PK 비교 분석 결과. (셀트리온 2019 EULAR 포스터 발표자료)
◇54주간 램시마SC의 안전성, 효능 관찰한 1상 결과도 발표.. 램시마SC 적정용량 근거
셀트리온은 이번에 공개된 Part 2 결과 이전에 류마티스관절염 환자를 대상으로 램시마SC제형의 PK와 효과, 전체적인 안전성을 확인, 평가한 Part 1 결과를 발표한 바 있다. 이번 EULAR 학회에서도 1년간의 임상1상 관찰결과를 공개했다.
28개 관절 중 6개 이상의 관절에서 질병이 진행중이고 C반응성단백의 혈중농도가 0.6mg/dL 이상인 류마티스환자 50명을 모집하고 0주와 2주에 램시마IV제형 3mg/kg를 투약했다. 이후 6주 시점에서 램시마IV 투약군, 램시마SC 90mg, 120mg, 180mg 투약군 등 총 4개의 코호트로 환자를 분류하고 약물을 적용해 54주까지 효과 및 안전성 등을 관찰했다.
PK 분석 결과, 6주 이후의 시점에서 램시마SC제형의 모든 적용군은 램시마IV 제형군보다 높은 혈중 농도를 유지했다. 이러한 결과는 2주마다 약물을 적용하는 SC제형의 투약시점과 관련이 있으며, SC제형을 적용했을 때 치료효과가 있는 일정농도를 유지하는 것이 더 편리할 가능성을 의미한다.
54주까지의 치료효과를 확인하기 위해 DAS28(CRP)와 ACR20으로 평가하고 적용군 별로 비교분석했다. 그 결과, DAS28 기준으로 54주 관찰시점에서 모든 SC제형 적용군이 IV제형 대비 더 높은 개선효과를 보였다. 램시마SC 90mg 적용군의 경우 14주까지는 타 적용군 대비 낮은 효과를 보였지만 22주 이후에는 IV제형보다 좋은 양상을 보였으며 54주 시점에서는 다른 용량의 램시마SC 적용군과 비슷한 수치를 보였다. ACR20의 경우, 램시마IV와 램시마SC제형 모두 비슷한 양상을 보이는 것으로 확인됐다.

▲램시마IV와 램시마SC 90mg, 120mg, 180mg 환자코호트의 DAS28 변화양상. (셀트리온 2019 EULAR 포스터 발표자료)
셀트리온은 안전성을 확인한 결과, 램시마SC 180mg 적용군에서만 치료와 관련된 심각한 이상반응이 관찰(2명)됐다고 밝혔다.
54주간 램시마IV형과 SC형의 PK-PD 모델링 데이터와 효과, 안전성 등을 비교한 결과, 이전에 공개한 30주 관찰 결과와 같이 IV제형과 SC제형간 비슷한 양상이 관찰됐으며 SC제형의 비열등성을 확인할 수 있었다. 또한 이러한 데이터들을 기반으로 램시마SC제형의 적정용량은 2주간격으로 120mg을 투여하는 것으로 설정됐다.
셀트리온 관계자는 "이번 유럽류마티스학회 참석자들에게 램시마SC와 램시마를 동시에 활용한 성공적인 임상 3상 결과를 첫 선보여 세계 의료진들로부터 많은 주목을 받았다"며 "셀트리온그룹은 연내 램시마SC의 유럽의약품청 승인이 기대됨에 따라 이번 학회를 계기로 본격적인 램시마SC의 학술 마케팅에 돌입하는 한편, 하반기 다양한 학회를 통해 세계 제약 시장에 당사 바이오의약품의 우수성과 편의성을 널리 홍보할 계획"이라고 밝혔다.







