기사본문
마이오반트, 'GnRH 길항제' 전립선암 3상 ‘반응률 96.7%’
입력 2019-11-20 15:20 수정 2019-11-20 15:20
바이오스펙테이터 서일 기자

마이오반트 사이언스(myovant science)는 경구용 GnRH(gonadotropin-release hormone) 수용체(receptor) 길항제(antagonist) 신약후보물질 '렐루골릭스(relugolix)'의 진행성 전립선암(advanced prostate cancer) 임상 3상(HERO study) 결과를 지난 19일(현지시간) 발표했다.
임상결과 1차종결점과 6개의 2차종결점을 충족했고, 마이오반트는 이번 데이터를 기반으로 2020년 2분기에 미국 식품의약국(FDA)에 신약신청서(new drug application, NDA)를 제출할 계획이다.
결과 발표에 따르면, 평가기준인 응답자를 5~48주까지 테스토스테론(testosterone) 농도 50ng/dL이하로 유지하는 것으로 기준삼아 분석한 결과, 렐루골릭스는 96.7%의 반응률(95% CI: 94.9%, 97.9%)을 보이며 1차종결점을 충족했다.
2차종결점 중 하나인 48주간 테스토스테론 억제 효과에서 렐루골릭스 그룹은 96.7%, 대조약인 기존 치료제 루프로라이드(lueporlide) 그룹은 88.8%로 그룹 간 7.9%포인트(95% CI: 4.1%, 11.8%) 차이를 나타내며 비열등성(non-inferiority)을 보였다.
그 외 2차종결점인 테스토스테론의 빠른 억제, 테스토스테론 심각한 억제, 전립선-특이적 항원(prostate-specific antigen, PSA) 억제, 여포자극호르몬(follicle-stimulating hormone) 억제에서 모두 통계적 유의미한 결과(p<0.0001)를 얻었다.
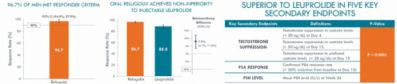
▲렐루골릭스 전립선암 임상 결과(마이오반트 홈페이지 참조)
렐루골릭스는 1일 1회 투여하는 경구용 GnRH 수용체 길항제로 전립선암을 발생시키는 주 원인인 고환 테스토스테론 생성을 감소시킨다. 다케다제약(Takeda Pharmaceutical)이 처음 렐루골릭스를 1일 1회 경구제로 개발해 2016년 마이오반트에게 아시아 국가를 제외한 지역에서 글로벌 임상 3상을 수행하고, 상용화할 수 있는 권리를 이전했다.
로이반트 사이언스(Roivant Sciences)의 자회사로 출발한 여성 질환, 전립선암 치료제를 개발회사인 마이오반트는 2019년 9월 일본 스미토모 다이니폰 제약(Sumitomo Dainippon Pharma)에 인수됐다.
한편, 마이오반트는 지난 7월 렐루골릭스 자궁근종 임상 3상(LIBERTY 2 study)에서 71.2% 반응률로 월경 출혈량을 감소시키며 1차, 2차 종결점을 충족했다고 발표했다. 이 결과를 바탕으로 올해 말까지 미국 FDA에 신약허가신청(NDA)를 제출할 계획이다.







