기사본문
엘리엠, ‘GABA 수용체’ 우울증 1상 중간 “긍정적”
입력 2022-10-07 13:16 수정 2022-10-07 13:16
바이오스펙테이터 서윤석 기자

미국 엘리엠 테라퓨틱스(Eliem Therapeutics) 5일(현지시간) GABA A 수용체 타깃 약물 ‘ETX-155’의 주요우울장애(major depression disease, MDD) 임상 1상에서 추가적인 약동학적(PK) 연구의 긍정적인 중간분석 결과를 발표했다.
발표에 따르면 엘리엠은 임상 1상에서 안전성과 내약성을 확인하고, 광과민성뇌전증(photosensitive epilepsy, PSE) 환자 3명을 대상으로 ETX-155 135mg을 투여한 개념입증(PoC) 임상 1b상 연구에서 50%이하의 낮은 약물노출(drug exposure)을 확인해 추가 연구를 진행해왔다.
그 결과 엘리엠은 42명의 임상참여자를 대상으로 진행한 추가임상에서 ETX-155 60mg의 약물노출 수준이 이전 진행한 임상에서의 ETX-155 60mg을 반복투여한 결과와 유사한 결과를 확인했다. 또 PSE 환자에게서 나타난 낮은 약물노출 수준은 변동성범위(moderate variability) 안에 있었다.
엘리엠은 현재 ETX-155 75mg를 투여해 내약성, PK 등을 분석하고 있다. 엘리엠은 이 결과를 바탕으로 내년 130명의 환자를 대상으로 주요우울장애(MDD) 임상 2a상을 진행할 계획이다.
안전성 측면에서 ETX-155 60mg 투여군의 부작용 발생비율은 58%(14/24명)으로 위약군 64%(7/11명)과 유사한 수준이었다.
ETX-155는 경구용 GABA A 수용체 양성 조절인자(positive allosteric modulator, PAM)로 시냅스 외부에 위치한 수용체인 GABA A의 신경스테로이드 부위에 결합해 가바성(GABAergic) 물질의 시냅스간 전달을 높여 뉴런의 흥분상태를 억제하고 안정화를 유도하는 기전이다.
이는 바이오젠(Biogen)이 지난 2020년 세이지(Sage)와 31억달러 규모로 사들인 약물 중 하나인 MDD 치료제 후보물질 ‘주라놀론(zuranolone, SAGE-217/BIIB125)’과 동일한 기전이다. 주라놀론은 임상3상에서 우울증 평가지표인 HAMD-17 점수를 개선하며 1차종결점을 충족시켰으나 치료 12일차 이후부터 효과가 감소해 18일 이후부터는 위약군과 차이를 보이지 못해 지속성에 한계를 보였다.
엘리엠은 ETX-155의 반감기가 40시간으로 기존 약물보다 길고, 음식섭취에 따른 약물노출 차이(food effect)가 없어 복용 편의성에서 차별화 된다는 설명이다.
밥 아젤비(Bob Azelby) 엘리엠 CEO는 “ETX-155의 적절한 수준의 약물노출(exposure) 등 약동학적 문제를 해결해 임상 2a상에 진입하기 위한 준비를 마쳤다”며 “임상 2a상을 통해 ETX-155의 효능과 안전성을 평가할 수 있을 것”이라고 말했다.
한편 엘리엠은 2018년 설립된 기업으로 지난해 5월 시리즈B로 6000만달러를 유치했다. 엘리엠은 주요우울장애 외에도 통증치료제 후보물질 'ETX-810' 임상 2상과 전임상 단계의 Kv7.2/3 포타슘채널 타깃 치료제 후보물질을 연구하고 있다.
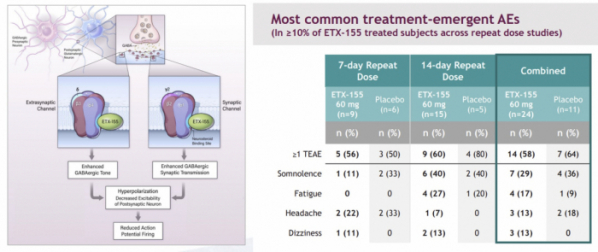
(엘리엠 IR 자료 참조)







