기사본문
메디프론 "내년부터 주력 파이프라인 임상 본격 진입"
입력 2016-09-27 09:43 수정 2016-09-27 09:43
바이오스펙테이터 장종원 기자
국내 바이오텍 메디프론 디비티의 주력 파이프라인인 신경병성 통증(Neuropathic Pain) 알츠하이머성 치매(Alzheimer’s disease) 치료제 및 진단기기 개발이 내년부터 속도를 낼 전망이다. 신경병성 통증 치료제는 유럽 1상에 알츠하이머 치료제는 국내 2상에 본격 진입할 전망이다.
27일 메디프론 디비티에 따르면 독일 그루넨탈(Grunenthal)에 4000만 유로에 기술이전한 신경병증 진통제 'MDR-16523'은 내년 유럽 1상에 진입할 계획이다. 현재 그루넨탈이 유럽의약품청(EMA)과 임상 승인 신청을 위한 사전 미팅을 진행 중이다.
MDR-16523은 효능이 마약성 진통제에 버금가고 부작용은 적다고 알려진 바닐로이드 수용체(TRPV1) 길항제다. 각종 부작용에다 악효 지속이 어려운 기존 (마약성) 의약품을 극복한 차세대 진통제로 부각받으면서 머크, GSK 일라이릴리 등 글로벌 제약사들이 신약 개발에 뛰어든 분야다. 하지만 임상 1~2상에서 환자에게 열이나는 이상발열 부작용으로 모두 중단했다.
메디프론과 그루넨탈 연구진은 발열기작을 규명하고 이상발열의 근본원인을 발견. 해결했고 약물 효능도 입증했다. 화이자가 바닐로이드 수용체(TRPV1)를 기반으로 신경병성 통증약 개발에 뛰어들었지만 메디프론보다 속도가 더디다. 신경병증 통증 치료제 시장은 2010년만 56억 5000만달러, 2020년에는 84억 2800만달러로 전망된다.
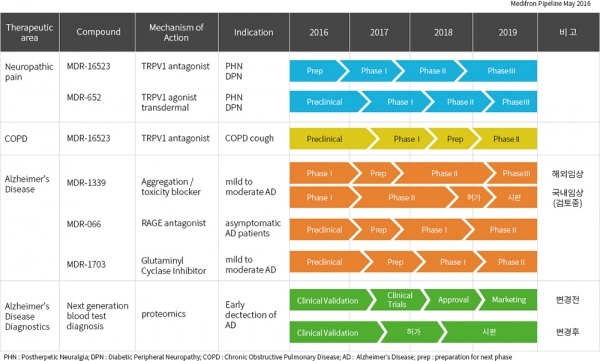
메디프론 관계자는 "독일 그루넨탈이 차세대 먹거리로 신경병증 통증 치료제를 선정하고 집중개발하고 있다"면서 "MDR-16523은 기존 리리카 등과 비교해 복용이 편리하고 부작용도 없으며 약효도 우수하다"고 강조했다. MDR-16523은 국내에서 패치제(MDR-652)로도 개발되고 있는데 최근 일본 제약회사와 물질이전 계약(MTA)를 맺었다.
올 연말 1상 완료 예정인 알츠하이머 치료제(MDR1339)는 국내 2상을 계획하고 있다. 최근 정부가 알츠하이머 신약에 대해 임상 2상 이후 출시를 허용하고 연구비도 지원하는 규제 완화책을 내놓으면서 속도가 붙었다. MDR1339은 치매 원인인 아밀로이드베타의 응집을 효과적으로 저해해 치료한다.
뇌혈관장벽(BBB)에 존재하는 RAGE(Receptor for Advance Glycation Endproduct)가 혈관 내 아밀로이드베타 단백질과 결합해 뇌안으로 옮기는 기능을 차단하는 MDR066은 2010년 2억 9000만달러에 '로슈’에 기술 이전돼 현재 전임상 진행중이다.
메디프론은 2011년 식약처로부터 반려받은 알츠하이머병 진단 키트도 개량해 재도전한다. 피 한방울로 90% 이상 정확도를 자랑한다. 반려 이후 릴리의 아미비드, GE의 비자밀, 피라말의 뉴라체크 등이 허가를 받으면서 치매 진단 키트 시장이 재주목받고 있다. 국내에서는 일진그룹 계열사인 알피니언이 한국과학기술연구원으로부터 관련 기술을 이전받아 개발 중이다.
메디프론 관계자는 "올해 임상 시험 등으로 타당성을 검증해 내년 국내 허가에 도전하겠다"고 말했다.







