기사본문
포티세븐, 'CD47 치료제' 악성 혈액암 대상 "ORR 92%"
입력 2019-12-11 07:13 수정 2019-12-11 08:39
바이오스펙테이터 서일 기자

악성 혈액암에 대해 높은 반응률과 완전관해를 보인 CD47 항체 치료제 후보물질의 임상 결과가 나왔다. 이 임상결과를 발표한 포티세븐(Fortyseven)의 주가는 발표한 후 전일 대비 110% 상승했다
포티세븐은 지난 9일(현지시간) 2019년 미국 혈액암학회(2019 American Society of Hematology, ASH)에서 ‘마그롤리맙(magrolimab)+아자시티딘(azacitidine)’ 병용요법으로 골수이형성증후군(Myelodysplastic Syndrome, MDS)과 급성 골수성 백혈병(Acute Myeloid Leukemia, AML)환자를 대상으로 진행 중인 임상 1b상 결과를 내놨다.
발표에 따르면 MDS 환자 대상 전체반응률(overall response rate, ORR)은 92%, 완전관해(complete response, CR)는 50%였고, AML 환자 대상으로는 ORR 64%, CR/Cri 55%를 보였다. 추가적으로, TP53 유전자 돌연변이를 가진 AML 환자 대상으로 ORR 78%, CR/CRi 77%의 결과를 내놨다.
마그롤리맙은 대식세포를 활성화하는 두가지 기전을 가진 CD47 항체 치료제다. 먼저 대식세포가 암세포를 인지하고 활성화하게 한다. 마그롤리맙은 암세포 CD47과 결합해 암세포의 ‘나를 먹지 말아줘(Don’t eat me)’ 신호를 저해한다. 추가적으로, 암세포와 결합한 마그롤리맙의 Fc 부분이 대식세포의 Fc 수용체와 결합해 암세포에 대한 대식작용을 촉진한다. 이런 기전은 다른 화학치료제, 면역항암제와 시너지 효과를 갖는다.
데이비드 샐먼(David Sallman) 모티프 암센터 연구소 임상연구원은 “MDS 환자를 치료하는 임상의로서 일부 환자에게만 적용이 가능한 표준치료제의 한계를 느끼고 있다”며 “75% 환자는 보조 치료나 증상 관찰만 받고 있다”고 전했다.
포티세븐은 기존에 치료받지 않은 MDS와 AML 환자를 대상으로 ‘마그롤리맙+아자시티딘’ 병용요법으로 치료를 진행했다. 기존 화학치료제인 아자시티딘은 MDS와 AML 환자에게 사용하는 치료제다.
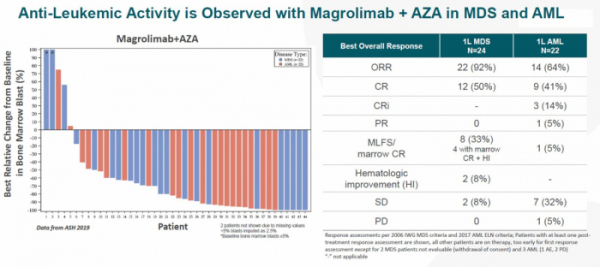
▲마그롤리맙 임상 결과(포티세븐 발표자료 참조)
마그롤리맙은 임상 1b상 결과에서 높은 반응률과 완전 관해를 보여줬다. 24명의 MDS환자를 한 분석에서 ORR 92%, CR 50%를 보였고, 22명의 AML 환자 분석에서 ORR 64%, CR 41% CRi는 14% 였다. CRi(complete remission with incomplete hematologic recovery)는 모든 CR기준을 충족시키지만, 혈액내 호중구나 혈소판 수치가 일정 기준치 이하를 보일 때 사용한다. CRi환자는 CR환자에 비해 치료효과가 상대적으로 떨어지는 경향을 보인다.
약물 반응은 평균적으로 1.9개월만에 MDS, AML 환자에서 나타났고, 평균 약물 효과 지속시간(Duration of respone, DOR)은 MDS 환자 6.4개월, AML 환자 8.4개월로, 환자들이 생존해 있어 중간값은 도출하지 못했다.
마그롤리맙은 특히 TP53 돌연변이 유전자를 가진 AML환자에서 더 효과적이었다. 포티세븐은 AML 환자에서 TP53 유전자 돌연변이 여부를 분석했다. 평가 가능한 TP53 돌연변이 유전자를 가진 AML 환자 9명에서 ORR 78%(7/9) CR 44%, CRi 33%를 보였다. 반응을 보인 환자 전부가 완전관해를 보인 것이다. TP53 돌연변이를 가지고 있는 AML 환자는 기존 치료법에 반응도 덜하고 치료 예후도 나쁘다.
한편, 포티세븐은 미국 식품의약국(FDA)과의 협의를 거쳐 변경한 프로토콜에 따라, 90명의 환자를 추가로 모집해 진행하는 임상 3상 결과를 기반으로 2021년 4분기 미국 FDA에 바이오의약품 허가신청서(Biologics License Application, BLA)를 제출할 계획이다. 포티세븐의 마그롤리맙은 지난 9월 미국 식품의약국(FDA)에 패스트트랙으로 지정된 바 있다.

▲포티세븐 파이프라인(포티세븐 발표자료 참조)







