기사본문
버텍스, '트리카프타' 첫 분기 매출 4.2억弗 "깜짝"
입력 2020-02-03 13:14 수정 2020-02-03 13:47
바이오스펙테이터 김성민 기자
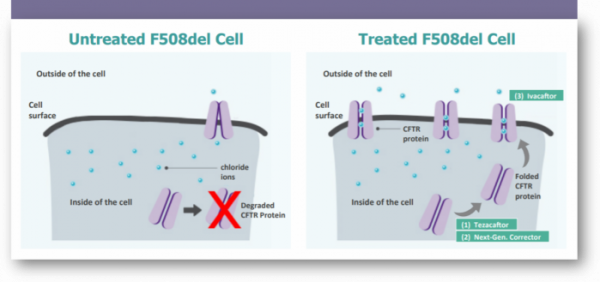
▲트리카프타(Trikafta) 삼중요법 작용 메커니즘, 회사 자료.
버텍스파마슈티컬(Vertex Pharmaceuticals)의 낭포성 섬유증 치료제 ‘트리카프타(Trikafta, elexacaftor/tezacaftor/ivacaftor)’가 지난해 10월 21일 미국 식품의약국(FDA) 승인받은지 9주만에 미국내 4분기 매출액이 4억2000만달러(한화로 약 5017억원)를 기록하는 놀라운 성과를 냈다. 당초 월스트리트가 예상했던 7000만달러보다 6배 높은 수치다. 버텍스는 낭포성섬유증 치료제 분야의 선두주자로, 치료대안이 없는 낭포성섬유증 치료제 신약을 출시한 최초의 회사다.
업계에 따르면 트리카프타는 최근 5년 동안 출시된 신약 가운데 가장 성공적인 출발을 보여주고 있다. 또한 4분기 낭포성섬유증 제품 전체 매출액 12억6000만달러에서 버텍스가 출시한 4번째 신약인 트리카프타가 가장 높은 비중을 차지했다. 트라카프타 비용은 4주 처방을 기준으로 2만4000달러며, 한해 비용은 31만1000달러로 고가의 치료제다.
트라카프타는 여러 면에서 업계의 주목을 받는 신약이다. 트라카프타는 FDA로부터 혁신신약지정을 받아 허가신청서 제출후 3개월만에 신약허가를 받았다. 예상보다 5개월 앞서 결정이 내려진 것. 유럽의약품청(EMA)에는 지난해 10월 판매허가신청서 제출(MAA)을 승인받아 검토 단계에 있다.
또 다른 장점은 넓은 환자군이다. 낭포성섬유증은 세포막에 있는 Cl- 이온 채널인 CTFR 유전자 변이로 인해 단백질 기능이 망가지면서 생기는 병으로 변이 종류만 2000개가 넘으며, 낭포성섬유증을 일으키는 127개의 변이 중 F508del이 가장 흔한 형태다. 버텍스는 CTFR 이온 단백질의 오작동 자체를 근본적으로 고치는 접근법으로 계속해서 치료 환자군을 확대하기 위해 포토폴리오를 확충하고 있다.... <계속>







