기사본문
국내 개발된 새로운 항암제·알츠하이머 치료제 후보들
입력 2016-10-13 08:21 수정 2016-10-13 08:44
바이오스펙테이터 장종원 기자, 조정민 기자

희귀난치병을 고치는 획기적인 신약으로의 변신을 꿈꾸며 기술이전을 기다리는 각종 신약 후보물질들이 공개됐다. 암 전이까지 억제하는 항암제 후보물질을 비롯해 두 개의 타깃으로 알츠하이머 치료에 접근하는 기전, 노인성 근감소증 등과 같은 새로운 시장을 겨냥한 물질 등이 소개됐다.
한국생명공학연구원은 12일 서울 강남구 역삼동 GS타워 25층에서 기술이전 설명회를 개최했다. 한국생명공학연구원 소속 연구원들이 도출한 신약후보물질을 바이오제약 기업들에 소개하고 기술이전을 논의하기 위해 마련된 행사다.시장성있고 잠재력을 가진 다양한 후보물질들이 참석자들의 관심을 끌었다.
◇벤프로페린 유도체, 항암 및 전이 억제 효과
먼저 권병목 한국생명공학연구원 책임연구원은 항암 및 암 전이 억제효과를 가진 물질 'MD164'를 소개했다.
암 세포가 성장하거나 이동이 일어날 때, 가지가 형성되는데 이를 사상위족(filopodia)이라 한다. 사상위족은 포민(formin)이라는 단백질이 세포 필라멘트의 일종인 액틴(actin)에 중합되거나 Arp2/3(Actin-related protein) 복합체의 형성 과정을 통해 만들어질 수 있다.
연구팀은 암 세포의 사상위족 형성에 핵심적인 역할을 하는 Arp2복합체를 차단하는 기능을 가진 벤프로페린 유도체 함유 물질인 MD164를 개발했다. 생체 외(In vitro)에서 간, 췌장 등 다양한 암세포를 이용해 실험한 결과 원발성 암의 성장 억제 뿐 아니라 암 전이도 억제되는 결과가 나왔다.
포민으로 위족을 형성하는 정상 세포는 타깃 범위에 들어가지 않으므로 특이적인 암 치료법으로 사용이 가능하다는 것도 동물 실험을 통해 확인했다.
MD164는 혈관 내피세포의 혈관 형성을 저해함으로 비정상적인 혈관 신생으로 야기되는 질환의 예방 및 치료에도 유용하게 사용될 수 있다는 설명이다.
권 연구원은 “종양 전이 및 재발 등을 예방, 억제하는 약물로 개발하거나 암세포 특이적인 타깃을 활용해 새로운 개념의 면역치료제 개발로 활용할 수 있다"면서 "기존 약물과 병용 투여를 통해 항암 효과를 높일 수 있다”고 강조했다.

◇막단백질 TM4SF5 간암·대장암의 새로운 타깃
한국생명공학연구원 면역치료제 융합연구단의 김세미 책임 연구원은 새로운 간암, 대장암 표적치료제 개발 기전을 소개했다.
간암은 간염바이러스, 알코올, 비만 등의 원인으로 간 섬유화, 간 경변 등이 발생하고 이후 진전돼 발생하는데 초기 발견이 어렵고 외과적 수술 이외의 치료법이 없는 상태다. 또한 높은 재발율과 사망률을 보이고 있어 치료제 개발이 시급하다.
김 연구원은 간암과 대장암 세포 표면에서 과발현 되는 것으로 알려진 막단백질 TM4SF5를 새로운 간암 치료 표적으로 삼았다. 이 단백질에 세포외도메인 EC2(extracellular domain2)의 항원결정기에 결합하는 특이적 항체를 선별해서 실험을 진행했다.
생체외 실험에서 간암세포(SNU-449Tp)와 대장암세포(HCT-116)의 확산을 10~20% 저해하는 결과를 보였고 동물 피부 표면에 간암세포를 피하 주사하는 방식의 실험에서 암 성장을 억제했다.
이 물질은 암 세포 표면에서 발현되는 TM4SF5에 결합해 세포 이물흡수(endocytosis)를 활성화하는 ADCC(Antibody dependent cellular cytotoxicity) 기전으로 암세포의 성장과 생존을 억제한다.
김 연구원은 “TM4SF5 양성 암이라면 간암, 대장암 뿐 아니라 폐암, 식도암 등으로 확장 적용할 수 있고 환자의 T 세포에 항체를 부착하는 방법의 CAR-T 치료법으로도 활용이 가능하다”고 말했다.
◇항암물질 CX-4945로 알츠하이머 치료 가능성
혈액암 등에서 발현하는 카제인 카이네이즈2(CK2) 등을 억제하는 물질인 CX-4945를 활용해 알츠하이머 치매 질환 치료에 활용하는 기술도 소개됐다.
알츠하이머의 신경병리적 현상은 노인반과 신경섬유 엉킴이다. 글로벌 제약사들은 각각의 타깃에 대해 신약개발을 진행 중인데 조성찬 한국생명공학연구원 선임연구원은 'Dyrk1A'라는 신규 타깃을 통해 노인반과 신경섬유 엉킴을 동시에 조절하는 기전을 밝혀냈다.
Dyrk1A는 신경 발달에 중요한 역할을 하는 인산화 효소로 21번 염색체의 다운증후군 위험부위에 유전자가 존재한다. 다운증후군 환자들이 알츠하이머 유사 증상을 보이는 것과 알츠하이머, 파킨슨 질환자들에게서 Dyrk1A 발현이 증가하는 것을 발견했다.
조 연구원은 이 Dyrk1A를 억제하는 물질로 CX-4945를 활용했다. 이는 Dyrk1A의 발현을 억제해 신경섬유 엉킴의 원인으로 알려진 Tau의 인산화와 집적(aggregation)을 감소시키는 기전으로 작용한다. 또 노인반의 전구물질인 APP의 인산화를 억제하는 효과를 보였다.
조 연구원은 “지금까지 DYRK1A의 억제물질로 알려진 것들 중 가장 강력한 억제력을 가진 물질로 억제활성이 약 20배나 우수하다”고 말했다.
◇부필 피리디늄 유도체로 근육약화 방지
노인성 근감소증 예방 및 치료를 위한 새로운 약물기전이 소개됐다. 나이듦에 따라 근육이 퇴화하는 노인성 근감소증은 일상생활 활동을 어렵게 할뿐 아니라 기초대사율을 저하시켜 2형 당뇨병 발생을 촉진시키기도 한다. 아직 질병이라는 인식이 부족하지만 미국에서 이달 노인성 근감소증에 질병코드를 부여해 앞으로 더 큰 시장을 열릴 것이라는 전망도 나온다.
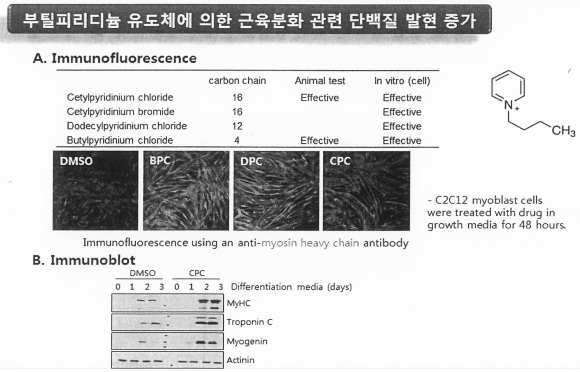
권기선 한국생명공학연구원 노화제어연구단장은 부필 피리디늄(Butylpyridinium) 유도체를 활용해 근원세포(myoblast)의 분화를 촉진시키는 기전을 소개했다. 이를 통해 근육 약화를 방지할 뿐 아니라 근육 기능을 개선할 수 있다는 것이다.
실제 실험 결과 부필피리디늄 유도체가 근육분화 관련 단백질 발현을 증가시키는 것을 확인했다. 역시 노화마우스에서 근력 향상 및 근육 증가를 관찰했다.
현재까지 노인성 근감소증으로 미국 FDA에 허가받은 치료제는 전무하다. 사노피, 머크 등이 근감소증 치료를 위해 Myostatin과 Activin receptor 등을 표적으로 하는 연구를 진행하고 있다.
권기선 단장은 "부필피리디늄 유도체는 노인성 근감소증, 희귀질환인 근이영양증 등에 활용될 수 있다"면서 "주름 개선을 위한 미용 치료제로서 가능성도 있다"고 설명했다.







