기사본문
'B형혈우병 유전자치료제' 유니큐어, 스파크-화이자 추격
입력 2019-02-12 08:10 수정 2020-02-02 20:51
바이오스펙테이터 서일 기자

유니큐어(Uniqure)가 B형혈우병(hemophilia B) 유전자 치료제의 임상2b상에 대한 긍정적 결과를 내놨다. 이번 결과는 경쟁관계에 있는 스파크(Spark)-화이자(Pfizer)의 유전자치료제와 비슷한 효능으로 업계는 두 경쟁사의 임상3상 결과를 주시하고 있다.
유니큐어는 지난 8일 체코 프라하에서 개최된 유럽 혈우병협회(EAHAD)에서 ‘AMT-061’ 임상2b상 임상결과 12주만에 3명 환자의 혈우병 응고단백질 FactorIX(FIX) 활성이 평균 정상의 38%로 증가했다고 발표했다.
이번 임상2b상 시험은 중증 혈우병 환자 3명에게 'AMT-061' 2x10^13 gc/kg을 단일 정맥 투여하는 방식으로 진행했다. 투여 후 16주가 지난 환자의 경우 정상의 48%, 14주인 경우 25%, 12주인 경우는 51%의 FIX 활성을 나타냈다. 3명 환자의 12주 시점 평균 FIX 활성은 정상의 38%였다. 이는 임상적으로 의미있는 개선이며 출혈을 보이거나 응고인자 FIX의 보완 치료가 필요한 환자는 없었다고 회사측은 설명했다.
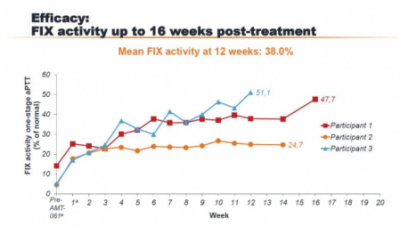
▲EAHAD 2019 'AMT-061' 임상 2b상 발표 자료
유니큐어는 2018년 11월 임상2b상 시험(NCT03489291)에서 환자에게 6주간 ‘AMT-061’ 2x10^13 gc/kg를 투여한 결과 FIX 활성이 정상의 31%였다고 밝힌 바 있다. 이번 결과는 6주간의 결과보다 향상됐음을 보여줬다.
매트 카푸스타(Matt Kapusta) 유니큐어 대표는 “AMT-061을 이용한 치료 목표는 모든 B형혈우병 환자들이 대체 요법과 면역반응의 위험없이 한번의 치료로 FIX 활성을 정상화하는 것”이라며 “이번 임상결과는 AMT-061이 목표를 달성할 수 있는 최초의 유전자 요법임을 보여주며, 올해 말까지 진행하는 임상3상의 결과를 추가할 것”이라고 말했다.
유니큐어는 지난주 초 임상 3상시험(NCT03569891)인 HOPE-B의 첫 환자에게 약물을 투여하였다. HOPE-B에서는 중증(severe) 및 중증도 증증(moderately severe)의 B형혈우병환자 56명에 동일한 용량(2x10^13 gc/kg)을 투여하여 안전성과 효능을 평가하게 된다.
AMT-061은 FIX를 과발현하는 FIX-Padua 변형체를 가진 아데노연관바이러스(Adeno-associated virus 5, AAV5) 기반의 유전자 치료제로 중증 B형혈우병환자 치료제이다. B형혈우병은 F9유전자 돌연변이에 의해 혈액응고인자 FIX이 결핍된 X염색체 연관 유전병이다. 혈우병 환자들은 정상의 경우보다 과도한 출혈과 원인을 알 수 없는 출혈, 관절과 근육에서의 출혈로 통증을 겪는다. 현재 가능한 치료로는 결핍된 응고인자 FIX를 주입하는 대체치료법(Replacement therapy)이 있다.
AAV 기반의 유전자 치료제는 체내의 항-AAV 중화항체에 의한 면역반응 때문에 어려움이 있었다. AMT-061은 항-AAV5 중화항체를 가진 사람에 주입하였을 때에도 효과적으로 유전자를 전달할 수 있다는 것을 확인하였다.
AMT-061은 미국 식품의약국(FDA)으로부터 혁신치료제(Breakthrough Therapy Designation)로 지정 받았고, 유럽 의약품청(EMA)에서 의약품의 신속심사를 위한 우선순위 의약품(Priority medicine, PRIME)를 허가 받았다.
유니큐어와 경쟁구도에 있는 화이자(Pfizer)와 스파크(Spark)는 AAV8 기반의 FIX 유전자 치료제 ‘SPK-9001’을 개발 중이다. ‘SPK-9001’은 임상1/2상(NCT02484092)에서 12주간 약물을 투여받은 환자에서 38~55%의 FIX 활성이 나타나는 것을 확인했다. 화이자는 임상3상(NCT03587116)을 진행하기 전 대조군 스터디로 6개월간 FIX 대체 치료법을 진행중이다.







