기사본문
에스페리온, 경구용 LDL-C 저하제 '넥슬리젯' FDA 승인
입력 2020-03-02 07:11 수정 2020-03-02 09:54
바이오스펙테이터 서윤석 기자

에스페리온(Esperion Pharmaceuticals)은 26일(현지시간) 미국 식품의약국(FDA)으로부터 저밀도 지단백 콜레스테롤(LDL-C)를 낮추는 경구용 비(非) 스타틴(non-statin)계 복합제 '넥슬리젯(NEXLIZET™)'의 신약 승인을 받았다고 밝혔다. 이형성 가족성 고콜레스테롤혈증(heterozygous familial hypercholesterolemia, HeFH)과 죽상 경화성 심혈관질환 atherosclerotic cardiovascular disease, ASCVD) 환자를 대상으로 한 LDL-C 저하제다.
에스페리온은 이에 앞서 지난주 경구용 콜레스테롤 저하제 ‘넥슬레톨(NEXLETOL™, bempedoic acid)’의 신약승인을 받았는데, 넥슬리젯은 넥슬레톨과 머크의 '제티아(Zetia, ezetimibe)' 10mg을 섞은 1일1회 경구용 복합제로 개발됐다.
넥슬레톨은 ACL(ATP Citrate Lyase)저해제로 간에서 콜레스테롤의 합성을 억제하며, 제티아는 위장관에서 발현하는 단백질인 NPC1L1(Niemann-Pick C1-like 1)을 저해해 장에서 콜레스테롤 흡수를 억제한다. 넥슬리젯은 간에서 콜레스테롤 합성을 저해하면서 동시에 장에서 콜레스테롤 흡수를 억제하는 상보적인 기전을 가진다.
넥슬리젯은 최고 용량의 스타틴으로 치료받고 있는 HeFH, ASCVD 환자가 추가적으로 저밀도 지단백 콜레스테롤(low-density lipoprotein cholesterol, LDL-C)를 낮추기 위해 사용하도록 승인받았다. 넥슬리젯은 오는 7월 시판될 예정으로 보험이 적용되는 환자의 경우 하루 10달러에 최대 3개월간 공급받을 수 있다.
단, 넥슬리젯이 심혈관계 이환률과 사망률에 미치는 영향 2022년까지 연구를 진행할 예정이다. 팀 메이레벤(Tim M. Mayleben) 에스페리온 CEO는 “넥슬리젯은 LDL 콜레스테롤을 낮추는데 승인된 첫 비-스타틴 복합체 약물(non-statin combination medicince)”이라고 말했다.
LDL 콜레스테롤은 혈액 내 농도가 높아지면 동맥에 축적돼 심장마비, 뇌졸중 등 심혈관계 질환을 유발한다. LDL 콜레스테롤 수치는 체내 100mg/dL 이하가 정상이며, 100~129mg/dL까지 건강상 문제가 발생하진 않는다. 현재 표준 치료법인 스타틴을 최대 용량으로 투여함에도 불구하고, 미국 내에서 약 1500만명의 ASCVD와 가족성 고콜레스테롤증(FH) 환자의 LDL 콜레스테롤을 가이드라인에 맞출 수가 없게 된다.
현재 ASCVD와 FH 환자의 LDL 콜레스테롤 저하제로 출시된 제품은 암젠(Amgen)의 '레파사(Repatha®, evolocumab)', 사노피(Sanofi)의 프랄런트(PRALUENT®, alirocumab)이 있다. 암젠의 레파사와 사노피의 프랄런트는 PCSK9 항체로 주 2회 투여해 LDL 콜레스테롤을 저하시킨다. 레파사는 LDL 콜레스테롤을 54-77%, 프랄런트는 44-66% 감소시킨 결과를 보였다. 레파사와 프랄런트의 1년 약가는 약 5850달러다.
여기에 올해 미 FDA 시판될 것으로 보이는 노바티스의 PCSK9 RNAi 치료제 '인클리시란(Inclisiran)'도 경쟁에 뛰어든다. 노바티스는 지난해 12월 미 FDA에 신약허가 신청서를 제출해 승인을 기다리고 있다. 인클리시란은 임상 3상(ORION-9, 10, 11)에서 FH 환자의 LDL 콜레스테롤을 50%, ASCVD 환자는 54-58% 감소시킨 결과를 보였다. 인클리시란은 연 2회 투여하며 1년 약가는 아직 미정이다.
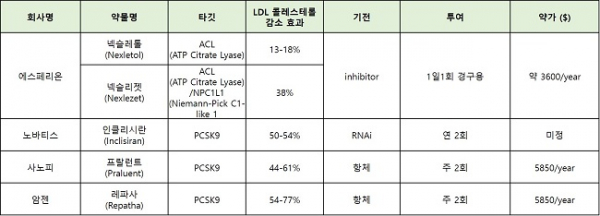
▲ASCVD, FH 환자 대상 LDL 콜레스테롤 저하제 가격과 효능 비교(각 회사 홈페이지 참조, 바이오스펙테이터 재구성)
넥슬리젯과 넥슬리톨의 임상3상 데이터는?
에스페리온의 발표에 따르면 넥슬리젯의 미 FDA 승인은 임상 3상(NCT03337308)에서 보인 LDL 콜레스테롤 감소효과와 지난주 승인받은 넥슬레톨(NEXLETOL, bempedoic acid) 상업화 임상 3상(NCT02666664) 결과가 바탕이 됐다.
에스페리온은 평균 LDL 콜레스테롤이 149.8 mg/dL인 301명의 고콜레스테롤 혈증 환자와 심혈관계질환 발생 고위험군 환자를 대상으로 넥슬리젯의 임상을 12주간 진행했다. 에스페리온은 12주차에 평가 가능한 임상 참여 환자들을 분석한 결과 LDL 콜레스테롤의 농도가 180mg의 벰페도익산 투여군(88명)에서 17.8% (P<0.001), 10mg의 에제티닙 투여군(86명)에서 23.2%(p<0.001), 넥슬리젯(86명)에서 36.2%(p<0.001) 감소한 결과를 확인했다. 위약군(41명)에서 LDL 콜레스테롤 농도가 1.8% 상승한 것과 비교하면 넥슬리젯에서 38%(p<0.001) 감소효과를 보였다. 에스페리온은 지난해 6월 임상 결과를 국제 학술지 EJPC(European Journal of Preventive Cardiology)에 게재했다(doi.org/10.1177/2047487319864671).
에스페리온은 넥스리젯의 승인에 앞서 지난 21일 LDL 콜레스테롤 저해제 넥슬레톨(NEXLETOL, bempedoic acid)의 미 FDA 승인을 받았다.
넥슬레톨 승인은 52주에 걸쳐 진행된 벰페도익산 임상 3상(NCT02666664) 결과에 기반해 이뤄졌다. 에스페리온은 2230명의 HeFH와 ASCVD 환자를 대상으로 위약군 742명과 넥슬레톨 투여군 1488명으로 나누어 52주간 임상을 진행했다. 임상에 참여한 환자의 평균 LDL 콜레스테롤 농도는 103.29mg/dL였으며 12주와 52주차에 결과를 평가했다. 에스페리온은 임상 진행 12주차에 LDL-C 농도가 기준점 대비 넥슬레톨 투여군이 16.5%(p<0.001), 52주차에 12.6%(p<0.001) 감소한 결과를 보였다. 위약군이 12주차에 기준점 대비 1.6%, 52주차에 1.0% 상승한 것과 비교하면 넥슬레톨 투여군에서 각각 18.1%, 13.6% 감소했다. 에스페리온은 지난해 3월 임상 결과를 정리해 국제 학술지 NEJM(The New England Journal of Medicine)에 개제했다(10.1056/NEJMoa1803917).
크리스티 발렌타인(Christie M. Ballantyne) 베일러의대 심장학과 교수 겸 에스페리온 임상 3상 집행위원은 “넥슬리젯은 최고 용량의 스타틴을 사용중인 환자들에게 LDL 콜레스테롤을 유의미하게 감소시켜 준다"며 "1일 1회 경구용 약물로 환자들이 사용하기 편리할 것”이라고 말했다.







