기사본문
MSD, 키트루다+TKI 병용 '신장암 1차치료제' 기대
입력 2019-02-14 06:40 수정 2020-02-02 20:53
바이오스펙테이터 서일 기자

‘키트루다(Keytruda)’가 신장암(renal cell carcinoma, RCC) 1차 치료제 승인에 한발 다가섰다. 신장암에서 키트루다와 화이자(Pfizer)의 타이로신 카이네이즈 억제제(Tyrosine kinase inhibitor, TKI)인 '인라이타(Inlyta, axitinib)'를 병용투여한 임상3상에서 PD-L1의 발현정도와 무관하게 1차 종결점인 전체 생존율(Overall survival, OS), 2차 종결점인 무진행 생존률(progression-free survival, PFS), 객관적반응률(Objective response rate, ORR)을 모두 달성하는 성공적 결과를 얻었다.
미국 머크(MSD)는 키트루다와 인라이타를 병용투여한 임상 3상 KEYNOTE-426(NCT02853331)의 중간분석 결과에서 이같은 데이터를 얻었다고 지난 11일 밝혔다. MSD는 오는 14일부터 16일 미국 샌프란시스코에서 열리는 2019 비뇨생식기 암 심포지엄(ASCO GU)에서 신장, 전립선, 방광에 해당하는 비뇨생식기 암 연구에서 새로운 병용 및 단독 요법 데이터를 발표할 예정이다.
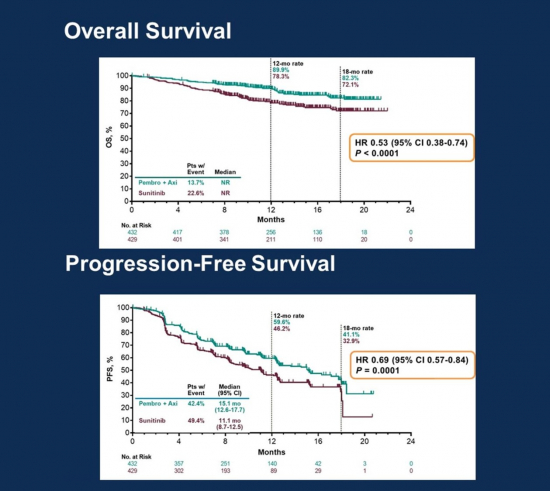
▲2019 ASCO GU 머크 발표 자료.
중간분석 결과에 따르면 키트루다와 액시티닙(axitinib)의 병용투여가 기존 1차치료제인 화이자의 TKI '수니티닙(sunitinib)' 단독투여에 비해 OS를 현저하게 개선해 사망위험을 47% 감소(HR 0.53 [95% CI 0.38-0.74]; P=0.0001)시켰다. 또한, PFS (HR 0.69 [95% CI 0.57-0.84]; P=0.0001)와 ORR (59.3% vs. 35.7%; P=0.0001)도 수니티닙과 비교하여 증가함을 보였다. 부작용은 단독투여와 큰 차이가 없었다. 치료관련 부작용은 3등급 이상에서 키트루다와 액시티닙은 62.9%, 수니티닙에서 58.1%이며, 처방중단비율은 각각 6.3%, 10.1%이다.... <계속>







