기사본문
온코닉, 'P-CAB' 위식도역류질환 3상 “美학회 논문”
입력 2024-08-21 09:59 수정 2024-08-21 09:59
바이오스펙테이터 신창민 기자

제일약품(Jeil Pharmaceutical)의 자회사인 온코닉테라퓨틱스(Onconic Therapeutics)는 21일 P-CAB 제제인 ‘자큐보(성분명: 자스타프라잔)’의 위식도역류질환 임상3상 결과가 미국 소화기학회(ACG)의 공식 학술지인 ‘American Journal of Gastroenterology’에 게재됐다고 밝혔다.
자큐보는 칼륨경쟁적 위산분비 저해제(P-CAB)로, 지난 4월 식품의약품안전처로부터 위식도역류질환 치료제로 시판허가를 받았으며, 국내 37호 신약이다.
이번 논문은 미란성 위식도역류질환 환자를 대상으로 자큐보와 대조군 프로톤펌프저해제(PPI) 계열 약물 ‘에스오메프라졸’의 효능 및 안전성 등을 비교평가한 임상3상의 연구결과이다.
이번 임상3상은 정훈용 서울아산병원 소화기내과 교수의 주도하에 국내 주요 병원에서 내시경상 미란성 위식도역류질환 환자 300명을 대상으로 이중눈가림, 무작위 배정을 통해 자큐보 20mg(149명), 대조군 에스오메프라졸 40mg(151명)으로 나누어 최대 8주 동안 약물을 투여했다.
8주 투여후 자큐보의 치료율은 97.9%로 대조군의 94.9% 대비 우수한 효능을 나타냈다. 특히 4주 투여시 자큐보의 치료율은 95.1%로 대조군에서 보인 87.7% 보다 7.44%높은 치료율을 보이며 신속하게 효능이 발휘되는 것을 확인했다.
부작용 분석결과 자큐보과 대조군 간의 통계적 차이는 없었다. 따라서 안전성 측면에서 오랫동안 표준치료제로 사용되어 왔던 에스오메프라졸과 비슷하며 특별한 부작용이 나타나지는 않을 것으로 기대된다고 회사는 설명했다.
현재 자큐보는 시판허가를 받은 적응증인 미란성 위식도역류질환뿐만 아니라, 위궤양 및 NSAID 유도성 소화성궤양 예방 적응증 등으로 확대하기 위한 임상시험을 진행하고 있다.
김존 온코닉테라퓨틱스 대표는 "세계적인 소화기 저널에 3상 시험 논문이 게재되어 전세계 의료진에게 K-신약인 자스타프라잔의 임상 결과를 공유하게 되어 기쁘다”며 "앞으로 한국 및 해외에서의 빠른 상용화를 위해 최선을 다할 것이며 적응증 확대에도 역량을 집중할 것"이라고 말했다.
한편 온코닉테라퓨틱스는 지난해 중국 제약기업 리브존파마슈티컬그룹(Livzon Pharmaceutical Group)에 중화권에서의 자스타프라잔 개발 및 상업화 권리를 1억2750만달러(한화 약1600억원) 규모로 라이선스아웃(L/O)한 바 있다.
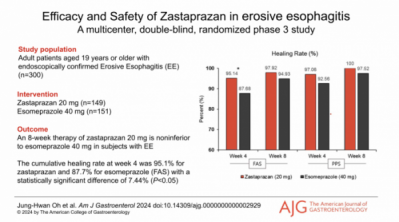
▲자큐보 3상 논문 효능결과(온코닉 제공)







