기사본문
셀트리온, '허쥬마' 급여등재 미루다 비싼 약가 획득한 사연
입력 2017-03-27 07:24 수정 2017-03-27 16:07
바이오스펙테이터 천승현 기자
국내 최초의 ‘허셉틴’ 바이오시밀러 ‘허쥬마’가 시판승인 3년만에 건강보험 급여목록에 이름을 올렸다. 셀트리온 측은 “특허문제 등의 이유로 발매 시기는 결정되지 않았다”는 입장이다. 그러나 허쥬마의 보험등재 시기를 늦추는 동안 바이오시밀러 약가우대 정책이 시행되면서 높은 가격을 받는 행운을 거머쥐었다.
27일 보건복지부에 따르면 셀트리온의 ‘허쥬마주150mg'과 ’허쥬마주440mg'이 내달부터 각각 1병에 37만2692원, 99만2812원의 보험상한가로 건강보험 급여 등재된다. 허쥬마는 로슈의 유방암치료제 ‘허셉틴’의 바이오시밀러 제품이다. 셀트리온 측은 “특허문제 등으로 아직 발매시기는 결정되지 않았고, 보험등재만 미리 한 상태다”라고 설명했다.
허쥬마는 국내 허가 이후 3년 만에 보험급여 목록에 등재됐다. 셀트리온은 지난 2014년 1월 식품의약품안전처로부터 허쥬마의 시판 승인을 받았지만 발매 시기는 미뤘다. 건강보험급여 등재도 시도하지 않았다.
셀트리온 측은 “해외에서 진행 중인 추가 임상시험이 완료되고, 특허문제도 해결된 이후 발매할 계획이다”라는 입장을 견지해왔다.
허쥬마는 오리지널인 허셉틴과 같이 조기유방암과 말기유방암에 사용할 수 있도록 허가받았다. 하지만 셀트리온은 허쥬마의 허가를 위해 말기 유방암 임상시험만 완료하고 허가를 받았다. 바이오시밀러의 경우 하나의 효능에 대해 오리지널과 동등하다는 사실만 입증되도 오리지널의 여러 효능을 모두 인정받을 수 있다.
셀트리온은 허쥬마가 중증 질환인 암 치료에 사용된다는 이유를 들어 임상자료를 보완한 후 발매하겠다는 전략을 세웠다. 허쥬마가 조기 유방암에 대한 임상자료가 확보되지 않은 상태에서 시장에 내놓아도 승산이 크지 않다는 이유에서다.
특허문제도 허쥬마 조기 발매의 걸림돌로 지목됐다. 셀트리온은 지난달 미국에서 허셉틴의 개발사 제넨텍을 상대로 특허무효 소송을 낸 상태다.
사실 허쥬마의 후속임상과 특허소송 등의 변수를 고려하지 않더라도 그동안 보험급여 등재를 미루는 것에 대해 이례적이라는 시선이 많았다. 통상 제약사들은 복제약(제네릭)의 발매시기를 결정하지 않더라도 보험약가를 미리 받는 전락을 구사했다. 식약처 시판승인 이후 미리 보험급여에 등재되면 추후 특허소송 결과 등의 변수에 따라 신속하게 발매할 수 있기 때문이다. 이에 대해 셀트리온 측은 “당장 국내에서 발매할 계획이 없기 때문에 보험약가도 받지 않았다”며 여유있는 입장을 견지했다.
셀트리온의 허쥬마 보험약가 등재 지연은 '고가 등재'이라는 예상치 못한 수혜로 돌아왔다. 정부의 바이오시밀러 약가우대 정책으로 종전에 비해 높은 약가를 받게 됐다.
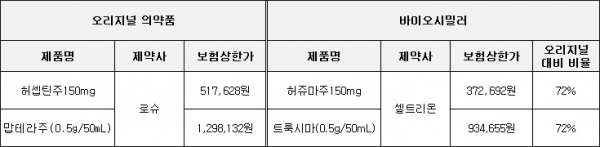
▲약가우대 적용받은 바이오시밀러 2종 약가현황(자료: 보건복지부·건강보험심사평가원)
허쥬마150mg의 약가 37만2692원은 허셉틴150mg(51만7618원)의 72%에 해당하는 수준이다. 허쥬마440mg은 오리지널 제품이 보험목록에 등재되지 않은 상태다.
보건복지부는 지난해 10월 약가제도 개편을 통해 국내 임상시험을 수행하고 혁신형제약기업이 개발하는 등의 요건을 충족한 제약사가 개발한 바이오시밀러는 오리지널 의약품 약가의 80%까지 받을 수 있도록 했다. 기존에는 오리지널의 70%까지 받을 수 있었지만 10%포인트 상향조정됐다.
만약 셀트리온이 허쥬마의 약가를 지난해 10월 이전에 받았더라면 보험약가는 오리지널의 70%인 36만2333원을 넘을 수 없었다.
셀트리온이 허쥬마의 보험급여 등재를 서두르지 않으면서 당초 기대하지 않았던 약가우대도 적용된 셈이다. 일각에서는 셀트리온이 허쥬마의 약가우대 적용을 위해 약가등재를 미뤘다는 의혹도 제기되지만 허쥬마가 허가받을 당시에는 바이오시밀러의 약가우대는 논의되기도 전이었다는 점에서 설득력이 떨어진다.
다만 셀트리온이 허쥬마의 약가를 오리지널의 80%가 아닌 72% 수준으로 책정한 이유는 오리지널 대비 가격경쟁력을 고려한 전략으로 분석된다.
셀트리온은 지난 2월 등재된 ‘맙테라’의 바이오시밀러 ‘트룩시마(0.5g/50mL)’의 보험약가를 93만4655원로 결정했는데, 오리지널 대비 72% 수준이다. 바이오시밀러가 발매되면 오리지널의 약가도 종전의 80% 수준으로 떨어지는데 오리지널과 바이오시밀러의 가격이 비슷하면 바이오시밀러가 경쟁력이 발휘하기 힘들다는 판단에 최고가보다 가격을 다소 내렸다.
지난해 10월 이전 발매된 셀트리온의 ‘램시마’, 삼성바이오에피스의 ‘브렌시스’와 ‘렌플렉시스’ 등 3종의 바이오시밀러 모두 특허 만료 전 오리지널의 65% 수준에서 보험약가를 결정했다.
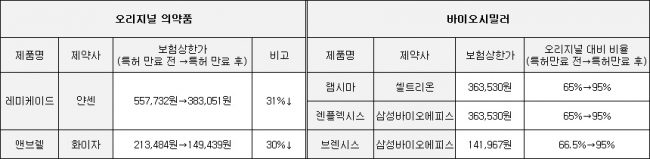
▲약가우대 시행 이전 등재된 바이오시밀러 약가현황(자료: 건강보험심사평가원)
트룩시마와 허쥬마의 보험약가는 특허만료 이후 오리지널 의약품(특허 만료 전 80%) 대비 90% 해당할 것으로 전망된다. 예전 약가제도와 비교시 더 높은 가격으로 판매하면서도 오리지널 대비 가격경쟁력은 더 높아진 셈이다.
결과적으로 셀트리온은 올해 2개의 바이오시밀러를 건강보험 급여목록에 이름을 올리면서 약가우대 혜택까지 받게 됐다. 지난해 10월 정부의 약가우대 정책 시행 이후 직접적으로 수혜를 입은 제품은 셀트리온의 바이오시밀러 2종 뿐이다.







