기사본문
가이드 RNA 말단 조작, 'CRISPR-Cpf1' 교정효율 높인다
입력 2018-10-04 13:01 수정 2018-10-04 13:01
바이오스펙테이터 이은아 기자

차세대 유전자교정 기술인 CRISPR-Cpf1 시스템의 효율을 높이는 방안이 제시됐다. 표적유전자와 결합하는 가이드 RNA의 말단에 유리디닐레이트(Uridinylate) 추가를 통해 Cpf1 단백질과 최적화된 CRISPR RNA간의 결합력을 높임으로써 높은 교정효율을 가지도록 했다.
한국생명공학연구원(생명연) 유전자교정연구센터 김용삼 박사 연구팀은 ‘네이쳐 커뮤니케이션지(Nature Communications)’에 ‘Highly efficient genome editing by CRISPR-Cpf1 using CRISPR RNA with a uridinylate-rich 3’-overhan)‘ 제목으로 최근 논문을 발표했다. 이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 바이오의료기술개발사업 및 국가과학기술연구회가 추진하는 창의형 융합연구사업(CAP)의 지원으로 수행됐다.
CRISPR-Cpf1 시스템은 RNA 가이드와 결합된 핵산분해 효소가 표적유전자를 인식해 교정한다는 점은 기존의 CRISPR-Cas9 시스템과 동일하다. 두 시스템은 염기서열을 인식하는 부위가 다르다. Cas9은 3’말단에 구아닌(G)이 많은 PAM(protospacer adjacent motif) 서열을 인식하는 반면, Cpf1은 5‘말단에 티민(T)이 많은 PAM 서열을 인식해 Cas9을 사용할 수 없는 표적서열에 활용할 수 있다.
Cpf1은 Cas9보다 상대적으로 크기가 작아 체내 전달이 용이하고 낮은 오프타깃(off-target) 효과를 가져 안정성이 높은 편으로 알려져있다. 다만 유전자교정 효율이 낮다는 단점이 있다.
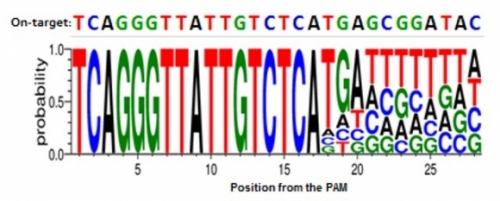
▲고효율 Cpf1을 구성하는 CRISPR RNA의 3’말단 서열. 표적 유전자와 결합하는 20개의 서열 뒤로는 표적유전자의 서열이 아닌 연속된 티민(T)이 가장 높은 효율을 가진다. (그림: 한국생명공학연구원 제공, 출처: doi: 10.1038/s41467-018-06129-w)
김 박사 연구팀은 별도의 화학적, 물리적 처리 없이 가이드 RNA의 3’-말단에 특정 염기서열을 추가함으로써 CRISPR-Cpf1 시스템의 효율을 높였다. 표적유전자와 결합하는 CRISPR RNA의 20개의 염기 이후의 3‘말단에 U4AU4를 추가했다. 그 결과 미생물 및 동물세포 수준에서 기존의 효율보다 최대 12배 향상된 교정 효율을 확인했다. 이때 오프타깃 효과는 변함없어 향상된 교정 효율성과 함께 특이성, 안정성을 동시에 갖춘 것을 확인했다.
연구팀은 총 115개의 유전자를 대상으로 한 대규모 검증을 통해 향상된 Cpf1의 효율이 Cas9 대비 비슷하거나 더 높은 교정 효율을 보임을 입증했다. 또 각각의 다른 표적유전자에 대해 Cas9과 Cpf1이 상이한 효율을 나타냈다.
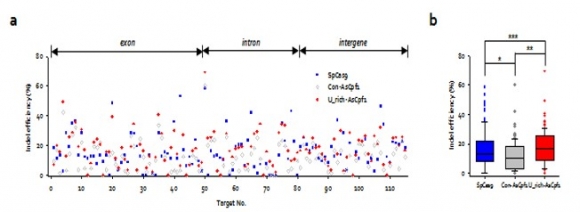
▲Cpf1과 기존의 CRISPR RNA(회색), 최적화된 길이의 우라실(U)을 붙인 CRISPR RNA(빨간색), 그리고 Cas9(파란색)으로 표적 유전자 115개를 교정한 효율을 나타낸 점도표(Dot-plot) (b) (a) 결과를 통계처리한 상자그림(Box-and whisker plot). (그림: 한국생명공학연구원 제공, 출처: doi: 10.1038/s41467-018-06129-w)
높아진 Cpf1 효율에 따른 작용기전도 밝혔다. Cpf1 단백질과 CRSIPR RNA간의 결합력을 비교한 결과 최적화된 CRISPR RNA가 기존의 것보다 뛰어난 결합력을 보이는 것을 확인했다. 이러한 특징은 Cas9에서는 보이지 않는 Cpf1의 고유한 성질임을 증명했다.
이번결과는 표적유전자에 따라 최적의 효율을 보이는 유전자가위가 다를 수 있음을 의미한다. 그동안 Cas9으로 교정하기 어려웠던 유전자를 Cpf1으로 대체 교정할 수 있는 가능성을 확인한 것이다. Cpf1의 향상된 교정 효율 및 낮은 오프타깃 효과로 유전자치료에 더욱 활용될 것으로 기대된다. 특히 Cpf1은 Cas9에 비해 상대적으로 작은 크기를 가져 AAV 등 바이러스를 통해 in-vivo 유전자치료에 적합할 것으로 보고 있다.
연구책임자인 김용삼 박사는 “이번연구 성과는 Cpf1의 장점인 낮은 오프타깃 효과는 유지하면서 간단한 방법으로 교정 효율을 향상시켰다는 것이 핵심”이라며 “Cpf1의 단점이었던 교정 효율을 높임으로써 다양한 유전자를 보다 쉽게 유전자교정하고, AAV와 같은 바이러스 전달체를 이용한 유전자치료에 대한 활용 가능성이 높아졌다”고 밝혔다.







