기사본문
제노포커스, '美 임상 예정' AMD신약 효능평가 공개
입력 2019-02-14 15:14 수정 2019-02-20 14:32
바이오스펙테이터 장종원 기자
제노포커스와 자회사 바이옴로직이 경구용 노인성 황반변성(Age-related Macular Degeneration, AMD) 신약후보물질 GF103의 비임상효능 평가 결과를 공개했다. GF103은 올해 연말 미국 식품의약국(FDA) 임상시험 승인을 계획중인 효소기반 신약후보물질이다.
제노포커스는 14일 "구강 투여하는 GF103의 비임상효능 평가, 기존 시판 안구주사 치료제인 아일리아(Eylea)와 동등한 효능을 보였다"고 밝혔다. 이번 연구는 GF103의 전임상 연구의 일환으로 부산백병원 안질환 T2B구축센터에서 진행됐다.
GF-103은 AMD의 주요 원인인 활성산소를 제거하는 항산화효소인 미생물 유래 SOD 효소 기반의 신약후보물질이다.
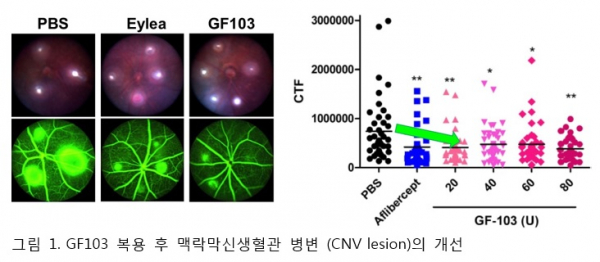
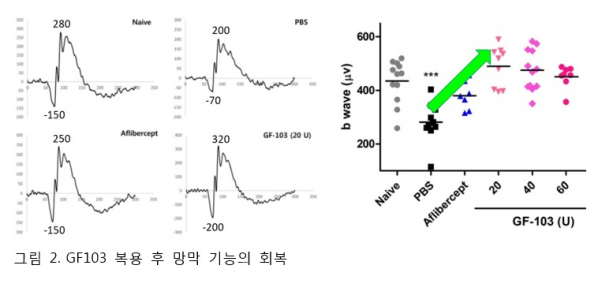
이번 효능 평가는 습성황반변성에 가장 널리 사용되는 레이저 유도 맥락막 신생혈관(laser-induced CNV) 마우스를 이용했다. GF103을 구강 투여시, 저농도군(20 unit/mouse)에서도 아일리아와 동등수준으로 맥락막신생혈관 병변(CNV lesion)이 개선됐다.(그림 1) 또한 GF103 투여는 CNV 병변 개선뿐 아니라 망막기능을 회복시킬 수 있을 가능성이 망막전위도검사 (Electroretinography)에서 확인됐다.(그림2)
또한 GF103 투여는 마우스 망막 내 혈관내피세포성장인자(VEGF) 농도를 항혈관내피성장인자(Anti-VEGF) 치료제인 아일리아와 동등한 수준으로 감소시켰으며, CNV 부위에서 세포자멸사(apoptosis) 정도를 억제했다. 이 외에도 CNV 부위에서 대식세포, 백혈구, ICAM-1과 같은 염증인자를 감소시킴으로써 염증 억제효과를 보였다.
맥락막 신생혈관에 의해 발병하는 습성 황반변성은 급격한 시력상실을 초래해 즉각적인 치료가 요구된다. 황반변성 환자수는 미국에만 900만명이 넘으며 노인 인구의 증가로 환자수는 세계적으로 점점 더 늘어나고 있다. 대표적 치료제인 아일리아와 루센티스는 2017년 기준 10조원 이상의 매출을 올리고 있지만 눈에 직접 주사를 하기 때문에 환자에게 고통스럽고, 장기간 사용시 효과가 감소하는 등의 단점이 있다.
제노포커스 관계자는 "올해 연말 미국 임상시험 승인을 목표로 FDA 사전미팅(Pre-ind meeting) 등을 준비하고 있다"면서 "치료제 개발이 완료되면 기존 안구주사 치료제를 대체하거니 빈도를 현저하게 낮출 수 있어 의미있는 신약이 될 것으로 기대한다"고 말했다.







