기사본문
'유니콘특례 1호' 보로노이, "5년내 FDA 가속승인 4개"
입력 2022-03-15 15:01 수정 2022-03-17 11:11
바이오스펙테이터 서윤석 기자
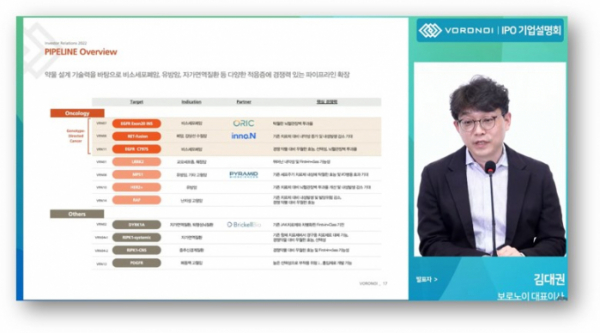
(보로노이 발표자료 참조)
국내 첫 유니콘 특례상장으로 이번달 30일 코스닥시장에 상장하는 보로노이(Voronoi)가 상장 후 5년내 달성하겠다는 '장밋빛' 청사진을 발표했다. 발암 원인 돌연변이가 명확히 밝혀진 암종(genotype-directed cancer, GDC)을 적응증으로 항암제 4종에 대해 미국 식품의약국(FDA)의 가속승인(accelerated approval)을 받겠다는 글로벌 빅파마 수준의 과감한(?) 목표다.
지난 2021년 신설된 유니콘 특례상장제도(시장평가 우수기업 특례)는 시가총액 5000억원 이상으로 예상되는 기업의 경우 전문평가기관 한 곳에서만 A등급 이상을 받으면 코스닥 상장예심청구 자격을 부여하는 제도다. 지난 2015년 설립된 보로노이는 2019년 기술특례를 위한 기술성평가에서 연이어 고배를 마신 후, 유니콘특례 1호 기업으로 방향을 전환했다.
김대권 보로노이 대표는 지난 14일 여의도에서 온라인으로 개최된 IPO 기업설명회를 통해 “높은 표적 선택성과 혈뇌장벽(BBB) 투과능을 가진 인산화효소(kinase) 선택적 저해제를 개발하고 있다”며 “5년내 파트너사에 라이선스아웃(L/O)한 파이프라인을 포함해 임상개발 파이프라인을 20개로 확대하고, 항암제 4개를 미국 FDA에서 가속승인 받는 것이 목표”라고 말했다.
미국 FDA의 가속승인은 심각한 질환에서 미충족의료수요(unmet medical need)를 채울 수 있는 대리 임상종결점(surrogate endpoint)을 바탕으로 치료제를 빠르게 시판하는 제도다. 승인받은 약물은 향후 추가임상을 거쳐 약물의 효능을 입증해야 하며, 입증하지 못할 경우 시판이 중지될 수 있다. 다른 치료약물이 해당 적응증에서 먼저 FDA의 정식 시판허가(fully approved)를 받을 경우 가속승인을 받을 수 없다.... <계속>







