기사본문
아펠리스, ‘C3 저해제’ GA 3상 장기추적 “병변감소”
입력 2022-03-21 13:51 수정 2022-03-21 13:51
바이오스펙테이터 서윤석 기자

아펠리스(Apellis)는 지난 16일(현지시간) C3 저해제 ‘엠파벨리(Empaveli, pegcetacoplan)’로 진행한 2개(OAKS, DERBY)의 지도모양위축증(geographic atrophy, GA) 3상 18개월간 장기 추적분석에서 GA병변면적을 유의미하게 감소시킨 긍정적인 결과를 발표했다.
아펠리스는 이번 데이터를 포함한 신약허가신청서(NDA)를 올해 2분기 미국 식품의약국(FDA)에 제출할 예정이다. 만약 엠파벨리가 승인받게 되면 GA로는 첫 약물이 된다. GA는 노인성 황반변성(age-related macular degeneration, AMD)의 중증형태로 실명의 주된 요인으로 알려져 있다.
페데리코 그로시(Federico Grossi) 아펠리스 CMO는 “엠파벨리는 대규모 환자군에서 GA병변면적을 지속적으로 감소시킨 유일한 치료법”이라며 “이번 데이터를 미국 식품의약국(FDA)에 제출해 전세계 GA 환자들에게 가능한 빨리 엠파벨리를 제공할 수 있기를 기대한다”고 말했다.
지난해 아펠리스는 약물투여 12개월차 분석결과 OAKS 임상(NCT03525600)에서는 GA병변을 유의미하게 개선한 반면, DERBY 임상(NCT03525613)에서는 GA병변면적을 근소한 p-value 차이로 개선시키지 못한 결과를 보인 바 있다.
이번 발표에 따르면 아펠리스는 18개월간 추적관찰한 결과 두 임상에서 모두 유의미한 GA병변면적 감소와 안전성 프로파일을 확인했다. 구체적으로 아펠리스는 2개의 임상 3상에서 총 1258명(OAKS 637명, DERBY 621명)의 GA 환자를 대상으로 엠파벨리와 위약을 월간 1회 또는 격월 1회씩 안구내주사(intravitreal injection) 방식으로 투여해 임상을 진행했다.
그 결과 아펠리스는 OAKS 임상에서 엠파벨리를 월간, 격월간 투여했을 때 GA병변면적이 각각 22%(p<0.0001), 16%(p=0.0018) 감소했다. DERBY 임상에서는 월간, 격월간 GA병변면적이 각각 13%(p=0.0254), 12%(p=0.0332) 감소한 결과를 확인했다.
18개월차의 안전성 프로파일은 12개월차 분석과 유사했으며, 망막혈관염(retinal vasculitis) 또는 망막 정맥폐색(retinal vein occlusion) 등의 사례는 보고되지 않았다.
아펠리스는 상세 분석결과를 향후 항회에서 발표할 예정이다.
한편 엠파벨리는 지난 2020년 발작성 야간혈색소뇨증(PNH) 치료제로 FDA로부터 승인받았다. 지난해 엠파벨리 매출은 1510만달러를 기록했다.
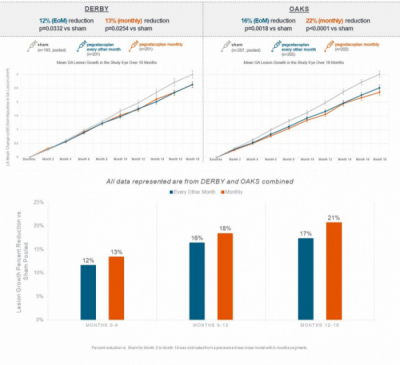
(아펠리스 자료 참조)







