기사본문
유틸렉스, ‘GPC3 CAR-T’ 간암 “국내 1상 IND 신청”
입력 2022-09-01 09:16 수정 2022-09-01 09:16
바이오스펙테이터 김성민 기자
표준요법 실패한 GPC3 발현 간암 대상

유틸렉스(Eutilex)가 진행성 간암 환자를 대상으로 GPC3 CAR-T 후보물질 ‘EU307’의 임상1상 임상시험계획서(IND)를 제출했다고 1일 공시했다. EU307은 사이토카인 IL-18을 분비하는 GPC3 CAR-T이다.
이번 임상1상은 표준요법에 실패한 GPC3 양성 진행성 간세포암(HCC) 환자를 대상으로 진행하며, 환자의 자가혈액 유래 GPC3 CAR-T를 투여해 안전성, 내약성, 예비 효능 등을 평가하는 시험이다.
임상은 12명에서 최대 15명을 대상으로 진행하며, EU307 용량별로 3~6명의 환자를 등록할 예정이다. 최종적으로 최대내약용량(MTD), 임상2상 권장용량(RP2D)을 확힌하게 된다. 임상은 국내 5개 대학병원에서 진행된다.
권병세 유틸렉스 대표는 “아직 뚜렷한 성과가 나타나지 않은 글로벌 고형암 CAR-T 치료제 시장에서, EU307을 통해 유틸렉스의 기술력을 소개할 수 있는 기회를 창출할 것”이라고 말했다.
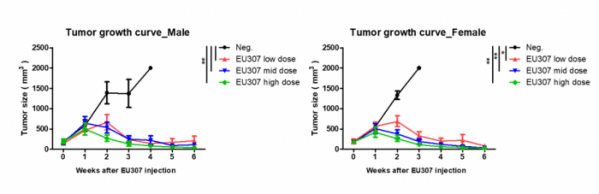
▲유틸렉스가 공개한 EU307 효능 데이터







