기사본문
한미약품 "다시 승부", 'HER2 저해제' "올 4분기 IND"
입력 2025-05-22 07:23 수정 2025-05-22 14:49
바이오스펙테이터 시카고(미국)=김성민 기자
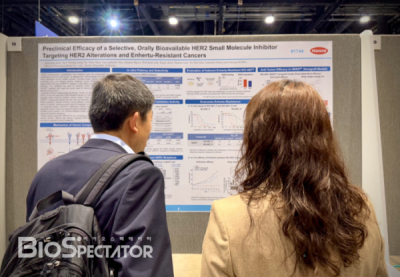
▲한미약품 ‘HM100714’ AACR 2025 포스터 발표현장서 전지영 한미약품 연구원(박사)이 설명을 진행하고 있다, 출처=바이오스펙테이터 촬영
‘포지오티닙(poziotinib)’의 한미약품(Hanmi Pharmaceutical)이 다시금 HER2 저해제로 비소세포폐암 영역에서 승부를 건다. 한미약품은 선택적 HER2 저해제 ‘HM100714’로 올해 4분기 임상시험계획서(IND)를 신청할 계획이다.
한미약품의 포지오티닙은 저분자화합물 기반 HER2 변이 비소세포폐암 치료제 개발에 가장 근접했던 약물로, HER2 엑손20 삽입변이(exon 20 insertion mutation) 환자에게서 효능을 보였지만 독성의 문턱을 넘지 못했다. 임상에서 EGFR 관련 약물 부작용으로 3등급 이상 발진(rash)이 49%, 3등급 이상 설사가 26%로 높게 관찰됐다. 이후 HER2 항체-약물접합체(ADC) ‘엔허투’가 2022년 미국 가속승인을 받으며 치료대안으로 등장했으나, 여전히 부작용 이슈가 있다.
이러한 가운데 베링거인겔하임의 HER2 TKI ‘존거티닙(zongertinib, BI 1810631)’의 등장으로 HER2 변이 비소세포폐암 치료제 개발 가능성이 비치고 있고, 미국 암연구학회(AACR 2025)에서 무진행생존기간(PFS) 12.4개월과 전체반응률(ORR) 71%라는 긍정적인 임상1/2상 결과를 업데이트했다. 존거티닙은 HER2 공유결합(covalent) TKI로, 야생형(WT) EGFR에 대한 선택성을 낮춰 임상에서 안전성 프로파일을 개선했다. 선택적 HER2 TKI 개발 경쟁이 한층 치열해지고 있다.
그러나 동시에 미충족수요도 새롭게 부각되고 있는데, 후발주자인 한미약품이 HM100714로 타깃하고 있는 영역이기도 하다. 크게 3가지 부분이다.... <계속>