기사본문
암젠, DLL3 타깃 CAR-T·BiTE 등 고형암 임상전략 공개
입력 2019-06-05 14:40 수정 2019-06-05 14:40
바이오스펙테이터 시카고(미국)=봉나은 기자
암젠이 소세포폐암 치료제를 위해 DLL3(Delta-like ligand 3)을 타깃한 다양한 항암제 임상개발 전략을 공개했다. 암젠은 2일(현지시간) 미국 시카고에서 열린 ‘2019 미국임상종양학회(ASCO)’에서 포스터 발표를 통해 DLL3 항원을 발현하는 소세포폐암 환자에게 CAR-T 및 BiTE(Bi-specific T-cell Engager) 후보물질을 적용한 임상 진행현황을 소개했다.
발표에 나선 Lauren Averett Byers MD 앤더슨 암센터(MD Anderson Cancer Center) 박사는 임상 결과를 발표하진 않았다. 1상이 작년 9월 시작해 아직 초기단계여서다. 그럼에도 이번 2019 ASCO 발표현장에서 암젠의 두 임상 현황이 주목받은 것은 고형암인 소세포폐암 치료를 위해 종양 조직에서 발현하는 'DLL3'를 T세포 기반 치료제의 강력한 타깃으로 보았다는 점이다.

▲Lauren Averett Byers MD 앤더슨 암센터(MD Anderson Cancer Center) 박사
소세포폐암(SCLC)은 화학항암제나 방사선 치료요법을 이용한 초기 치료에 민감하게 반응을 보인다. 그러나 다시 병이 재발해 신속하게 진행되고, 치료제에 저항성을 보이기도 하는 공격적인 신경내분비 종양(Neuroendocrine tumor)으로 완치가 어렵다.
폐 신경내분비 세포의 발달과 소세포폐암 조직의 성장에 관여하는 Notch 신호전달 기전은 소세포폐암에서 신경내분비 작용의 차이를 나타내게 하는 주요 기작으로 작용한다. 이러한 Notch 수용체의 리간드중 하나인 DLL3는 소세포폐암 환자의 약 85%에게서 발현되는 것으로 알려져, 이를 면역항암제 치료 타깃으로 주목하는 연구가 늘고있다.
1) 항 DLL3 CAR-T ‘AMG 119’
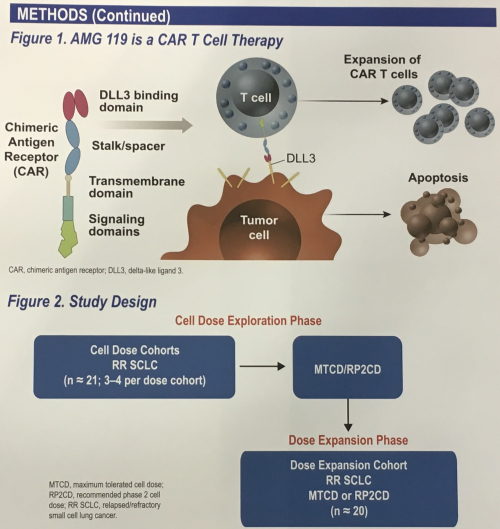
▲AMG 119 CAR-T 세포 구조 및 임상 디자인(암젠 2019 ASCO 발표 포스터)
먼저 'AMG 119'는 체외에서 DLL3 항원 표적의 CAR(Chimeric Antigen Receptor)를 발현하도록 설계한 환자의 자가 T세포 치료제다. 암젠은 in vitro 실험에서 AMG 119 CAR-T 세포가 DLL3를 발현하는 소세포폐암 세포를 사멸시키고, in vivo 소세포폐암 이종이식(Xenograft) 동물모델에서 종양의 성장을 저해하는 것을 확인했다.
암젠은 이번 ASCO에서 1회 이상 백금기반 화학항암제에 대한 치료 경험이 있으며, DLL3 항원을 발현하는 재발성/불응성 소세포폐암(SCLC) 환자에게 항 DLL3 CAR-T 후보물질 ‘AMG 119’를 단일투여하는 임상 1상(NCT03392064)의 진행 현황을 발표했다.
암젠은 이번 임상의 1차 종결점으로 AMG 119의 안전성과 내약성을 평가하고, 최대 허용 세포 용량(MTCD)이나 임상 2상 권고용량(RP2CD)을 확정할 예정이다. 2차 종결점으로는 항종양 활성, AMG 119의 증식 및 지속성에 대한 예비 효능, 치료 후 생검을 통해 종양 내부에 AMG 119가 침투했는지를 확인할 계획이다. 현재 임상은 환자 41명을 대상으로 하고 있다. 이중 21명은 AMG 119 투여 용량별로 나뉘어 ‘세포 용량 탐구 단계(Cell Dose Exploration Phase)’를 거쳐 MTCD와 RP2CD 설정을 돕고, 나머지 20명은 ‘용량 확대 단계(Dose Expansion Phase)’를 거쳐 MTCD나 RP2CD 설정을 도울 예정이다.
2) 항 DLL3 BiTE(Bi-specific T-cell Engager) ‘AMG 757’
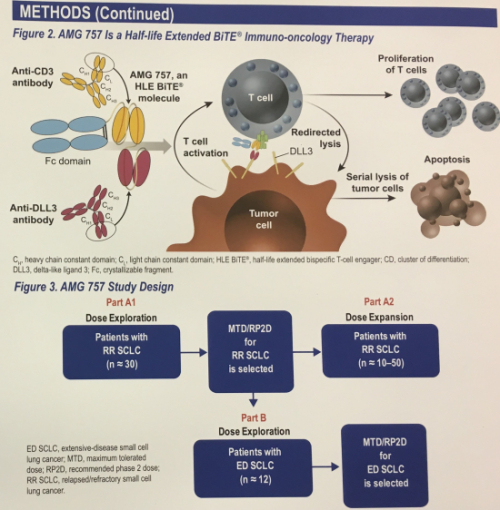
▲AMG 757 BiTE 구조 및 임상 디자인(암젠 2019 ASCO 발표 포스터)
암젠은 암 항원과 환자의 T세포를 연결시켜 T세포를 암 조직으로 끌어들이는 BiTE 플랫폼을 자체 개발했다. 이 플랫폼 기술을 적용한 BiTE 치료제 AMG 757은 DLL3를 발현하는 암세포와 CD3를 발현하는 T 세포를 연결시키도록 고안됐으며, 반감기를 연장시킨 형태로 개발됐다. 암젠은 AMG757을 이용해 T세포를 매개로 암세포 용해를 유도할 수 있고, 더불어 T 세포를 증식시켜 암 치료를 도울 수 있다고 설명했다. 암젠은 in vitro 실험에서 AMG 757이 소세포폐암 세포주를 사멸시키는 특성을 가지며, SHP-77 인간 소세포폐암 이종이식 동물모델에서 종양의 성장을 저해한다고 확인했다. 필리핀 원숭이(Cynomolgus monkey)모델에서는 다용량 독성 테스트를 진행해 AMG757이 잘 통제되고 조직손상에 대한 피해를 일으키지도 않았다고 확인했다.
암젠은 또 이번 2019 ASCO에서 1회 이상 백금기반 화학항암제에 대한 치료 경험이 있는 재발성/불응성 소세포폐암(SCLC) 환자에게 DLL3 타깃 BiTE 치료제 후보물질 ‘AMG 757’을 2주간격으로 1회씩 정맥투여하는 임상 1상(NCT03319940)의 진행 현황을 소개했다. 포스터 발표 현장에는 암젠의 Marie-Anne Damiette Smit 박사가 발표자로 나섰다.

▲암젠 Marie-Anne Damiette Smit 박사
암젠은 이번 임상의 1차 종결점으로 AMG 757의 최대 허용용량(MTD)이나 임상 2상 권고용량(RP2CD)을 설정하기 위해 안전성과 내약성을 평가할 예정이다. 2차 종결점으로는 약동학적(PK) 특성을 알아보고, 예비 항종양 활성을 평가할 계획이다. ‘용량 탐구 단계(Dose Exploration Phase)’에서 용량 제한 독성을 확인하기 위해 AMG 757 투여 후 28일동안 환자를 모니터링하고, ‘용량 확대 단계(Dose Expansion Phase)’에서는 MTD나 RP2CD를 확정하며, 나아가 안전성과 효능 데이터를 분석할 계획이다.
한편, 암젠은 2019 ASCO 현장에 차려진 부스에서 다양한 방법으로 암젠의 BiTE 플랫폼 기술을 소개하기도 했다. 미국 시카고 McCormick 학회장 밖 현지 거리에서도 BiTE를 알리는 광고들을 쉽게 찾아볼 수 있었다.

▲2019 ASCO 암젠 부스 현장







