기사본문
셀트리온, '고농도 휴미라 시밀러' "내년초 EMA 허가신청"
입력 2019-11-11 09:53 수정 2019-11-11 09:53
바이오스펙테이터 장종원 기자
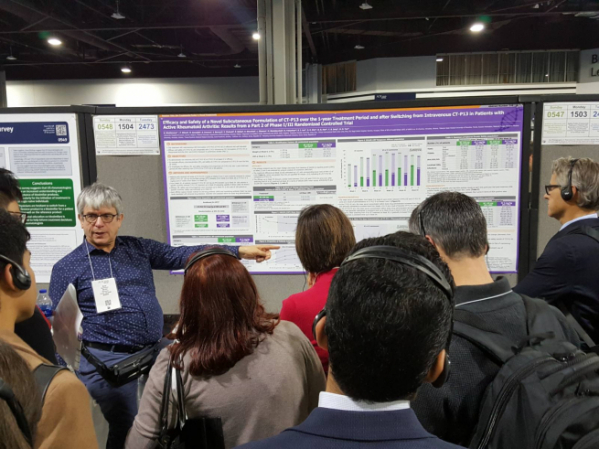
▲2019 ACR 학회 CT-P17 및 램시마SC 임상 결과 포스터 발표 현장. 셀트리온 제공.
셀트리온이 고농도 제형의 휴미라 바이오시밀러 ‘CT-P17’의 임상 1상 결과를 처음으로 공개했다. CT-P17은 현재 글로벌 임상 3상을 진행 중으로 셀트리온은 2020년 초 유럽의약품청(EMA)에 고농도 제형 최초의 휴미라 바이오시밀러로 허가를 신청할 계획이다.
셀트리온은 10일(현지시간) 미국 애틀란타에서 개최된 2019 미국류마티스학회(American College of Rheumatology, ACR)에서 자가면역질환 치료제 휴미라(Humira, 성분 아달리무맙) 바이오시밀러 ‘CT-P17’ 임상 1상 결과를 공개했다고 밝혔다.
CT-P17은 글로벌 매출 1위(지난해 기준 약 23조원)의 블록버스터 의약품인 휴미라의 바이오시밀러로, 셀트리온은 기존 바이오시밀러와 차별화한 전략으로 투여량을 줄여 환자 편의성을 강조한 고농도 제형으로 개발해 왔다. 현재 고농도 제형으로는 셀트리온 바이오시밀러가 유일한 것으로 알려지고 있다.
셀트리온 관계자는 "CT-P17은 셀트리온의 임상 개발 및 생산 노하우를 바탕으로 원가경쟁력을 확보했고, 기존 휴미라 바이오시밀러와 달리 주사 시 통증을 유발할 수 있는 구연산염을 제거한 CF(Citrate Free) 제형으로 개발되고 있어 경쟁 제품 대비 충분한 시장 경쟁력을 갖췄다"고 설명했다.
셀트리온은 이번 ACR에서 휴미라와 안전성 및 약동학을 직접 비교하기 위해 류마티스 관절염 환자 30명을 대상으로 휴미라 및 CT-P17을 처방하고, 투약 후 120일 간의 안전성과 약동학을 비교한 임상 1상 결과를 발표했다. 그 결과 CT-P17 투여군과 휴미라 투여군에서 유사한 결과를 도출하며, CT-P17과 휴미라의 유사성을 확인했다.
셀트리온은 현재 진행 중인 글로벌 임상 3상이 완료되는 내년 초 유럽의약품청에 CT-P17의 시판허가 신청 절차에 돌입한다는 계획이다.
CT-P17 글로벌 임상에 참여한 캐나다 마운트 시나이 병원 류마티스내과 전문의 키스톤(Keystone) 교수는 "CT-P17은 전 세계 매출 1위의 블록버스터 의약품인 휴미라를 고농도 제형으로 개발해 여타 제품 대비 경쟁력을 갖춘 만큼, 추후 시장에 선보인다면 의료진과 환자들에게 매력적이고 가치 있는 치료 옵션이 될 전망"이라고 말했다.
한편 셀트리온은 이번 학회를 통해 세계 최초 인플릭시맙 피하주사 제형인 '램시마SC'의 류마티스 관절염(RA) 적응증에 대한 1년여에 걸친 1·3상 장기 임상 결과도 함께 발표했다. 셀트리온 관계자는 "EMA 허가를 앞둔 램시마SC의 경우, 램시마IV와 함께 인플릭시맙 시장의 의료계 니즈를 바탕으로 한 듀얼 포뮬레이션 전략으로 포지셔닝하는 만큼, 앞으로 셀트리온이 휴미라 바이오시밀러 CT-P17까지 제품군을 확보하게 되면, 전 세계 45조원 규모 자가면역질환 치료제 경쟁에서 가장 강력한 포트폴리오를 갖춘 글로벌 바이오기업으로 자리매김할 것”이라고 말했다.