기사본문
中 '렘데시비르' 3상 2건 중단.."환자모집 한계"
입력 2020-04-16 12:54 수정 2020-04-17 14:38
바이오스펙테이터 봉나은 기자

중국에서 진행하던 코로나19 치료제 개발을 위한 길리어드(Gilead Sciences)의 '렘데시비르(remdesivir)' 임상 3상이 연이어 중단됐다.
중국 현지 코로나19 환자가 급감하면서 임상 참여자를 모집하기 어려워졌다는게 연구팀이 밝힌 3상 중단 이유이지만 이 소식이 알려진 이후 렘데시비르 개발사 길리어드 주가가 하락하는 등 우려섞인 시선도 나오고 있다.
16일 미국 임상정보사이트 'ClinicalTrials.gov'에 따르면 중국 수도의과대학(Capital Medical University)와 중국 의학과학원(Chinese Academy of Medical Sciences)은 지난 2월 개시한 코로나19 환자 대상 렘데시비르 3상을 일시 중단했다(Suspended).
이번 임상은 중일우호병원(China-Japan Friendship Hospital)에서 경증 및 중등도 수준의 코로나19 성인 환자 308명을 대상으로 렘데시비르의 효능 및 안전성을 평가하는 3상이었다(NCT04252664).
임상 중단 사유는 '코로나19가 잘 관리되고 있어 적합한 환자를 모집할 수 없다'였다. 당초 이 연구는 이달말 최종 마무리돼 결과를 발표할 예정이었다.
중국 연구진은 이에 앞서 같은 이유로 중증 코로나19 성인 환자 237명을 대상으로 한 첫번째 중국 3상(NCT04257656)도 중단(Terminated)한 바 있다. 이 연구는 지난 10일 임상을 마무리할 계획이었다. Daniel O’Day 길리어드 사이언스 대표는 최근 발표문을 통해 환자 등록 문제로 중증 코로나19 환자 대상의 중국 임상이 중단된 것을 보고받았다고 3상 중단 사실을 재확인했다.
이에 따라 코로나19 치료를 위한 렘데시비르의 유효성과 안전성은 길리어드와 미국 연구진이 진행하는 임상 결과를 통해서 확인 가능하게 됐다. 길리어드는 중등도 코로나19 환자 1600명 대상 임상 3상(NCT04292730), 중증 코로나19 환자 2400명 대상 임상 3상(NCT04292899)을 전세계에서 진행하고 있다.
길리어드는 이달말 중증 환자 대상 임상의 예비 분석 결과를 공개할 것으로 알려졌다. 또한 미국 국립 알러지감염병연구소(NIAID)가 진행하는 렘데시비르 임상의 초기 데이터도 5월 말 발표될 예정이다.
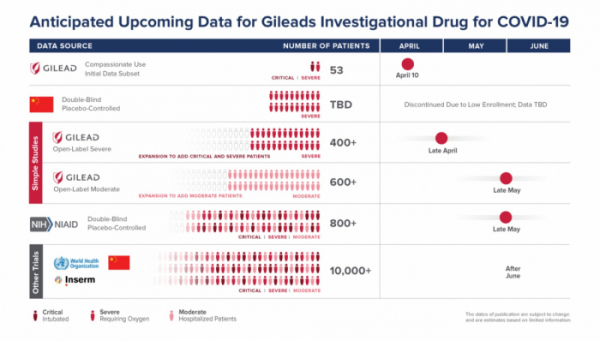
▲렘데시비르 임상 일정(길리어드 사이언스)
한편, 미국, 유럽(프랑스, 이탈리아, 스페인, 네덜란드 등), 캐나다, 일본 의료진은 지난 10일 길리어드의 지원을 받아 중증 코로나19 환자에게 치료목적으로 렘데시비르를 사용한 결과를 국제학술지 ‘NEJM’에 발표했다(doi: 10.1056/NEJMoa2007016).
1회 이상 렘데시비르를 투여받은 환자 61명 중 분석 가능한 53명의 데이터를 확인한 결과, 18일간(중간값) 추적관찰 했을 때 환자의 약 68%(36/53명)에서 증상(oxygen-support class)이 개선됐으며, 약 47%(25/53명)는 상태가 호전돼 퇴원한 것으로 나타났다. 렘데시비르에 대한 사망률은 약 13%(7/53명)였다. 비록 환자 수가 적고, 치료목적의 긴급사용에 대한 임상 결과로 타 연구 데이터와 직접비교할 수 없지만, 일부 환자에게서 가능성을 보였다는 점에서 주목을 받았다.