기사본문
알로비어, 2.76억弗 IPO..”HSCT후 감염증 T세포치료제”
입력 2020-08-03 15:30 수정 2020-08-03 15:30
바이오스펙테이터 서윤석 기자

미국 바이오벤처 알로비어(Allovir)가 미국 나스닥(Nasdaq) 기업공개(IPO)를 통해 약 2억7600만달러 규모의 자금조달에 성공했다. 알로비어는 조혈모세포 이식(HSCT) 후의 바이러스 감염증을 예방 및 치료하기 위한 동종유래 T세포 치료제를 개발하고 있다.
알로비어는 지난달 30일(현지시간) IPO를 통해 주당 17달러에 1630만주를 공모하며 2억7625만달러를 조달했다고 밝혔다. 알로비어의 주식은 나스닥에서 ‘ALVR’로 거래되며, 상장 첫날 25.39달러로 49% 상승해 마감했다.
알로비어는 바이러스별로 특이적인 항원을 인식하는 동종유래 T세포(allogeneic T cell)를 사용해 조혈모세포 이식후 발생하는 바이러스 감염을 예방하거나 치료하는 컨셉의 치료제(viral specific T cell, VST)를 개발한다. 알로비어는 조혈모세포 이식 환자의 90%에서 잠복해있던 바이러스가 재활성화되며, 활성화된 바이러스는 입원이 필요한 다발성 장기부전을 유발할 수 있다고 설명했다. 조혈모세포 이식후 바이러스 감염으로 인해 20%이상이 사망하며, 현재 이식후 바이러스 감염에 대한 승인된 약물은 없는 상황이다.
미국 증권거래위원회(SEC) 자료에 따르면 알로비어는 선도물질인 ‘비라일람-M(Viralyam-M, AVLR105)’을 비롯해 ALVR106, ALVR107, ALVR108, AVLR109 등을 개발하는데 공모한 자금을 사용할 계획이다.
알로비어의 선도물질인 비라일람-M은 조혈모세포 이식 후 BK바이러스, CMV(Cytomegalovirus), AdV(adenovirus), EBV( Epstein-Barr virus), HHV-6(Human herpesvirus 6)의 감염에 대한 치료제 후보물질이다. 알로비어는 58명의 환자를 대상으로 진행한 개념입증(POC) 임상 2상에서 93%의 환자가 임상반응을 보인 결과를 확인했다고 밝혔으며, 2021년까지 상업화 임상 3상을 진행할 계획이다.
또, 동종유래 조혈모세포 이식 후 바이러스 감염에 의해 발생하는 출혈성 방광염(hemorrhagic cystitis)을 대상으로 2020년 4분기 상업화 임상 3상을 진행할 계획이다. 알로비어는 출혈성 방광염을 가진 환자의 치사율(mortality)은 23.3%(vs 19.2%)로 출혈성 방광염이 없는 환자보다 높다고 설명했다.
ALVR109는 코로나19에 대한 치료제로 베일러의대(Baylor College of Medicine)와 개발을 진행하고 있으며 2020년 말 탑라인 결과를 확인할 것으로 예상하고 있다. 알로비어는 건강한 사람과 비교해 코로나19 환자에서 T세포 수가 감소해 있는 것을 확인했으며, ALVR109를 투여했을 때 신종코로나바이러스(SARS-CoV-2)를 특이적으로 용해(specific lysis) 시켰다고 설명했다.
알로비어의 ALVR106은 RSV(respiratory syncytial virus), 인플루엔자, PIV(Parainfluenza Virus), hMPV(human metapneumovirus)를 대상으로 2020년 하반기에 임상 1/2상을 시작할 계획이다.
마지막으로 ALVR107과 ALVR108은 각각 B형간염(HBV), HHV-8에 대한 치료제 후보물질로 2021년 하반기 임상허가신청서를 제출할 계획이다.
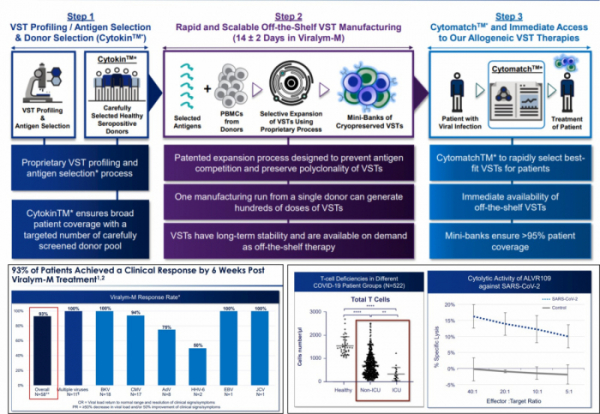
▲바이러스 특이적 T세포(VST) 제작과정 및 임상 결과 (알로비어 발표자료 참조)







