기사본문
국내 최초 유전자치료제 ‘인보사케이’ 시판 승인
입력 2017-07-12 08:29 수정 2017-07-12 09:10
바이오스펙테이터 천승현 기자
코오롱생명과학이 개발한 국내 최초의 유전자치료제 ‘인보사케이'가 국내 시판승인을 받았다.
식품의약품안전처는 무릎 골관절염치료제로 개발된 국내 처음 개발된 유전자치료제 신약 ‘인보사케이주’를 12일 허가한다고 밝혔다. 유전자치료제는 유전물질 발현에 영향을 주기 위하여 투여하는 유전물질 또는 유전물질이 변형되거나 도입된 세포를 함유하고 있는 의약품을 말한다.
▲코오롱생명과학 '인보사'
인보사케이는 약물치료나 물리치료에도 불구하고 통증 등이 지속되는 중등도 무릎 골관절염환자의 치료 용도로 무릎관절강내 1회 주사하도록 허가받았다. 코오롱생명과학은 지난해 7월 인보사케이의 허가신청서를 접수한지 1년 만에 식약처의 안전성·유효성 검증을 통과했다.
인보사케이는 항염증 작용을 나타내는 ‘TGF-β1 유전자’가 도입된 동종연골유래연골세포를 주성분으로 하는 약물이다. 국내제약사가 개발한 29번째 신약이다.
식약처는 “현재까지 미국, 유럽 등 주요 제약선진국이 허가한 유전자치료제는 4개 품목으로 면역결핍질환, 유전질환이나 항암치료를 목적으로 사용되며, 퇴행성 질환인 무릎 골관절염 치료를 위한 유전자치료제는 인보사케이주가 처음이다”라고 설명했다.
식약처는 인보사케이를 허가·심사하는 단계에서 △해당제품 투여 후 통증과 관절기능 개선 정도 △연골 구조 개선 효과 △제품 투여 후 발생하는 이상반응 △제품 투여 후 장기추적조사를 통해 뒤늦게 나타나는 이상반응 등 자료를 중점적으로 검토했고 중앙약사심의위원회의 자문을 거쳐 최종 허가를 결정했다.
인보사케이는 중등도의 무릎 골관절염 환자를 대상으로 해당 제품을 1회 주사하고 1년 후 환자가 느끼는 무릎 통증 개선정도와 운동이나 일상생활 등에서의 기능 개선정도를 대조군(생리식염수 투여군)과 비교한 결과 유효성을 입증했다. 기능 개선은 무릎관절 부위의 뻣뻣함·부종 등 증상 정도, 뛰기, 테니스 등 운동가능 정도, 계단오르기 장보기 등 일상생활에서의 활동 가능 정도 등을 종합해 평가한다.
다만 손상된 연골 재생 등 구조 개선 효과는 MRI 등을 통해 확인 시 대조군과 차이를 보이지 않았다.
인보사케이의 안전성 측면에서는 주사부위 국소반응(통증, 부종 등)과 전신반응(열감, 두드러기 등) 평가에서 안전했고 인보사케이를 투여한 100여명 환자 각각을 3∼10년간 별도로 추적 조사한 임상시험에서 지연 반응(종양, TGF-β1 농도 상승 등) 등을 평가한 결과에서도 안전한 것으로 나타났다.
식약처 관계자는 "2014년부터 바이오업체의 개발을 지원하기 위해 마중물사업을 운영하고 있으며, 이번 유전자치료제도 ‘마중물사업’을 통해 품질관리 기준 설정 등에 대한 밀착상담을 받아 개발 과정 중 시행착오를 최소화 할 수 있었다"라고 말했다.
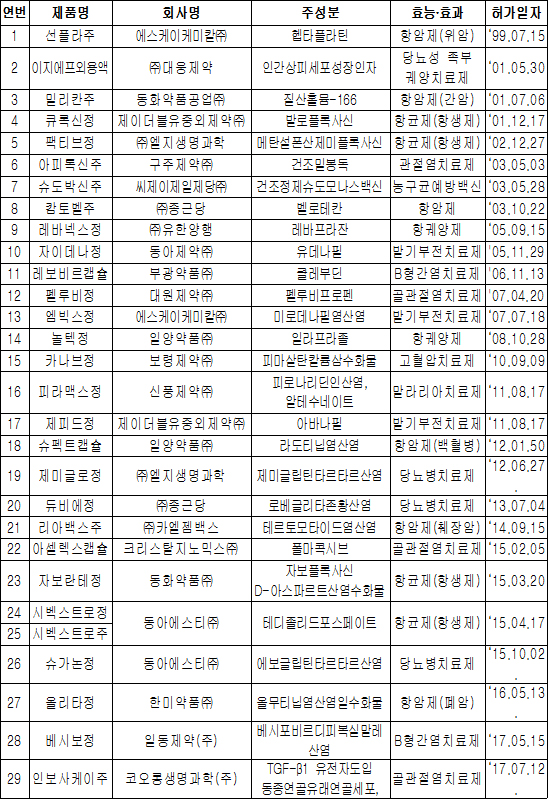
▲국내개발 신약 현황(자료: 식품의약품안전처)







